Léková Forma: Injekční
Lékařsky přezkoumány Drugs.com. Naposledy aktualizován dne 22. Května 2020.
- Overview
- Side Effects
- Dosage
- Professional
- Interactions
- More
FOR USE IN NERVE AGENT POISONING ONLY
A Sterile Solution For Intramuscular Use Only
Rx Only
- Pralidoxime Chloride Description
- Pralidoxim-Chlorid – Klinická Farmakologie
- Indikace a Využití pro Pralidoxim-Chlorid
- kontraindikace
- Varování
- bezpečnostní Opatření
- Obecně:
- Informace pro Pacienty:
- laboratorní testy:
- lékové interakce:
- karcinogeneze, Mutagenóza, porucha Fertility:
- těhotenství
- kojící matka:
- pediatrické použití:
- Nežádoucí Účinky
- zneužívání drog a závislost
- Předávkování
- Projevy Předávkování:
- Léčba Předávkování:
- Acute Toxicity:
- Pralidoxim-Chlorid Dávkování a způsob Podání
- návod k použití:
- jak se Pralidoxim chlorid dodává
- Hlavní Displej – Pralidoxim Chloridu sodného na Injekci 300 mg Label
- Více o pralidoxim
- Spotřebitelské zdroje
- Odborné zdroje
- Související léčba vodítka
Pralidoxime Chloride Description
Pralidoxime Chloride Injection (auto-injector) provides Pralidoxime Chloride in a sterile solution for intramuscular injection.
Každá předplněná auto-injector poskytuje dávku protilátky, Pralidoxim-Chlorid v samostatná jednotka, speciálně konstruované pro automatické self – nebo buddy-správy vojenského personálu. Pralidoxim v auto-injektor může být také podáván kvalifikovaným civilní pracovníky zasahující v případě nouze, kteří mají odpovídající vzdělání v na místě, rozpoznání a léčba nervových agent intoxikace v případě náhodného uvolnění nervových agent. Doporučeným postupem (viz dávkování a podání) je injekce obsahu autoinjektoru do svalů vnějšího stehna.
po aktivaci autoinjektoru musí být prázdný obal řádně zlikvidován (viz dávkování a podání), nemůže být znovu naplněn ani nemůže být vysunuta vyčnívající jehla.
Když jsou aktivovány, každé auto-vstřikovač dávkuje 600 mg Pralidoxim Chloridu sodného ve 2 mL sterilní roztok obsahující 20 mg/mL benzylalkohol, 11.26 mg/mL glycin ve Vodě pro Injekce, USP. PH se upraví kyselinou chlorovodíkovou. Rozsah pH je 2,0-3,0. Přípravek neobsahuje pyrogen.
Pralidoximchlorid je reaktivátor cholinesterázy.
Chemický název: 2-formyl-1 methylpyridiniumchlorid oxim(pyridin-2-aldoxim methochlorid). Označuje se také jako 2-Pam chlorid.
Strukturní Vzorec:
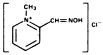
Pralidoxim-Chlorid vyskytuje jako bez zápachu, bílé, nonhygroscopic, krystalický prášek, který je rozpustný ve vodě v rozsahu 1 g za méně než 1 mL. Stabilní na vzduchu, taje mezi 215°C a 225°C, s rozkladem.
specifická aktivita léčiva spočívá v 2-formyl-1 methylpyridiniovém iontu a je nezávislá na konkrétní použité soli. Chlorid je výhodný z důvodu fyziologické kompatibility, vynikající rozpustnosti ve vodě při všech teplotách a vysoké účinnosti na gram díky své nízké (173) molekulové hmotnosti.
Pralidoxim-Chlorid – Klinická Farmakologie
Pralidoxim-Chlorid je cholinesterázy reactivator.
hlavní akce pralidoxim je aktivovat cholinesterázy (hlavně mimo centrální nervový systém), který byl inaktivován fosforylací kvůli organofosfátový pesticid nebo související sloučeniny. Destrukce nahromaděného acetylcholinu pak může pokračovat a neuromuskulární spoje budou opět fungovat normálně. Pralidoxim také zpomaluje proces „stárnutí“ fosforylované cholinesterázy na nereaktivovatelnou formu a detoxikuje určité organofosfáty přímou chemickou reakcí. Lék má svůj nejkritičtější účinek při zmírnění paralýzy svalů dýchání. Protože pralidoxim je méně účinný při zmírnění deprese dýchacího centra, Atropin je vždy vyžadován současně, aby blokoval účinek nahromaděného acetylcholinu v tomto místě. Pralidoxim zmírňuje muskarinové příznaky a symptomy, slinění, bronchospazmus atd., ale tato akce je relativně nedůležitá, protože Atropin je pro tento účel adekvátní.
Pralidoxim je distribuován v extracelulární vodě, není vázán na plazmatické bílkoviny. Lék se rychle vylučuje močí částečně nezměněný a částečně jako metabolit produkovaný játry. V důsledku toho má pralidoxim relativně krátkodobý účinek a může být zapotřebí opakovaných dávek, zejména tam, kde existují důkazy o pokračující absorpci jedu.
minimální terapeutické koncentrace pralidoxim v plazmě je 4 µg/mL, tato úroveň je dosaženo v asi 16 minut po jedné injekci 600 mg Pralidoxim-Chlorid. Zdánlivý poločas Pralidoximchloridu je 74-77 minut.
To bylo hlásil, že doplňkové použití oxim cholinesterázy reactivators (např. pralidoxim) snižuje výskyt a závažnost vývojové vady holka embrya vystavena takové známé teratogeny jako parathion, bidrin, karbacholem a neostigmin. Ukázalo se, že tento ochranný účinek oximů souvisí s dávkou.
Indikace a Využití pro Pralidoxim-Chlorid
auto-injector pro Pralidoxim-Chlorid je speciálně určen pro intramuskulární použití jako doplněk k atropinu při léčení otrav nervovými látkami s inhibitory aktivity.
kontraindikace
autoinjektor Pralidoxim chloridu je kontraindikován u pacientů s přecitlivělostí na jakoukoli složku přípravku.
Varování
Pralidoxim není účinný v léčbě otravy v důsledku fosfor, anorganické fosfáty nebo organofosfáty ne s inhibitory aktivity.
bezpečnostní Opatření
Obecně:
Pralidoxim byl velmi dobře snášen ve většině případů, ale je třeba mít na paměti, že zoufalý stav organofosfáty-otrávený pacient bude obecně masku takové drobné známky a příznaky, jako byly zaznamenány u zdravých jedinců.
protože se pralidoxim vylučuje močí, snížení funkce ledvin povede ke zvýšení hladiny léčiva v krvi. Dávka pralidoximu by tedy měla být snížena za přítomnosti renální insuficience.
Informace pro Pacienty:
Pralidoxim-Chlorid auto-injektor by měl být self – nebo buddy-spravuje vojenský personál nebo podáván kvalifikovaným civilní pracovníky zasahující v případě nouze pouze po těchto událostech došlo:
– jedinec má oblékl masku po uznání existence chemické látky, nebezpečí v jeho okolí – některé nebo všechny symptomy nervového plynu citované níže jsou přítomny: nevysvětlitelné výtok z nosu, pocit tlaku na hrudi s dýchacími potížemi označila žáků oka, rozostřené vidění, slinění, nadměrné pocení, nevolnost, zvracení a břišní křeče, nedobrovolné močení a defekace škubání, cukání, a ohromující bolest hlavy, ospalost, kóma, křeče, zastavení dýchání
Vhodné kroky musí být přijata, aby se ujistili, že personál vybaven auto-injektory pochopit jejich označení a použití, včetně přezkumu příznaky otravy a provoz auto-injector.
laboratorní testy:
léčba otravy organofosfátem by měla být zahájena bez čekání na výsledky laboratorních testů. Měření červených krvinek, plazmatické cholinesterázy a paranitrofenolu v moči (v případě expozice parathionu) může být užitečné při potvrzení diagnózy a po průběhu onemocnění. Snížení koncentrace cholinesterázy v červených krvinkách pod 50% normálu bylo pozorováno pouze při otravě esterem organofosfátu.
lékové interakce:
Když atropin a pralidoxim jsou použity společně, známky atropinization (návaly horka, mydriáza, tachykardie, sucho v ústech a nosu), může dojít dříve, než by se dalo očekávat, když atropin je používán sám. To platí zejména v případě, že celková dávka atropinu byla velká a podávání pralidoximu bylo zpožděno.2, 3, 4
při léčbě otravy anticholesterinázou je třeba mít na paměti následující opatření, i když nenesou přímo použití pralidoximu; od barbituráty jsou potencovány na anticholinesterázy, oni by měl být používán opatrně v léčbě křeče; morfin, teofylin, aminofylin, sukcinylcholin, reser-borovice, a fenothiazin-typ sedativa je třeba se vyhnout u pacientů s otravu organofosfáty.
karcinogeneze, Mutagenóza, porucha Fertility:
Od Pralidoxim-Chlorid auto-injector je indikován pro krátkodobé nouzové použití, žádné vyšetřování jeho potenciálu karcinogeneze, mutageneze, nebo poruchy fertility nebyly provedeny výrobcem nebo uvádí v literatuře.
těhotenství
reprodukční studie na zvířatech nebyly s pralidoximem provedeny. Rovněž není známo, zda pralidoxim může způsobit poškození plodu, pokud je podáván těhotné ženě, nebo může ovlivnit reprodukční schopnost. Pralidoxim by měl být podáván těhotné ženě, pouze pokud je to nezbytně nutné.
kojící matka:
není známo, zda se tento lék vylučuje do mateřského mléka. Protože se mnoho léků vylučuje do mateřského mléka, je třeba při podávání pralidoximu kojící ženě postupovat opatrně.
pediatrické použití:
bezpečnost a účinnost u dětí nebyla stanovena.
Nežádoucí Účinky
Čtyřicet až 60 minut po intramuskulární injekci, mírné až středně silné bolesti se mohou vyskytnout v místě vpichu.
Pralidoxim může způsobit rozmazané vidění, diplopie a zhoršení ubytování, závratě, bolesti hlavy, ospalost, nevolnost, tachykardie, zvýšený systolický a diastolický krevní tlak, zrychlené dýchání, svalová slabost, pokud je podáván parenterálně normální dobrovolníků, kteří nebyli vystaveni cholinesterázy jedy. U pacientů je velmi obtížné odlišit toxické účinky vyvolané atropinem nebo organofosfátovými sloučeninami od účinků léčiva.
Zvýšení AST a/nebo ALT hladiny enzymu byly pozorovány u 1 ze 6 zdravých dobrovolníků vzhledem 1200 mg Pralidoxim-Chlorid intramuskulárně, a ve 4 z 6 dobrovolníků vzhledem 1800 mg intramuskulárně. Hladiny se vrátily k normálu přibližně za 2 týdny. Přechodné zvýšení kreatinfosfokinázy bylo pozorováno u všech normálních dobrovolníků, kterým byl podáván lék. Jediná intramuskulární injekce 330 mg v 1 mL u králíků způsobila myonekrózu, zánět a krvácení.
Pokud se atropin a pralidoxim užívají společně, mohou se příznaky atropinizace objevit dříve, než by se dalo očekávat, pokud se atropin používá samostatně. To platí zejména v případě, že celková dávka atropinu byla velká a podávání pralidoximu bylo zpožděno.2, 3, 4 vzrušení a manické chování bezprostředně po obnovení vědomí byly hlášeny v několika případech. Podobné chování se však vyskytlo v případech otravy organofosfátem, které nebyly léčeny pralidoximem.3, 5, 6
zneužívání drog a závislost
Pralidoxim chlorid nepodléhá zneužívání a nemá žádný známý potenciál závislosti.
Předávkování
Projevy Předávkování:
Pozorována u normálních jedinců pouze: závratě, rozmazané vidění, diplopie, bolesti hlavy, poruchy ubytování, nevolnost, mírná tachykardie. V terapii bylo obtížné odlišit vedlejší účinky způsobené lékem od vedlejších účinků způsobených účinky jedu.
Léčba Předávkování:
Umělé dýchání a další podpůrná léčba by měla být podávána podle potřeby.
Acute Toxicity:
i.v.—man TDLo: 14 mg/kg (toxic effects: CNS) i.v.— rat LD50: 96 mg/kg i.m.—rat LD50: 150 mg/kg oral—mouse LD50: 4100 mg/kg i.p.—mouse LD50: 155 mg/kg i.v.—mouse LD50: 90 mg/kg i.m.—mouse LD50: 180 mg/kg i.v.—rabbit LD50: 95 mg/kg i.m.—guinea pig LD50: 168 mg/kg
Pralidoxim-Chlorid Dávkování a způsob Podání
Vystavení nervových agentů vlastnit aktivity cholinesterázy (organofosfáty typu)
v PŘÍPADĚ MÍRNÉ—bolest hlavy, rozmazané vidění, mírné muskarinové příznaky
STŘEDNĚ TĚŽKOU PŘÍPAD nadměrné pocení, slzení, slinění, průjem, tlak na hrudi
Pro optimální reaktivovat organofosfáty-inhibované cholinesterázy, atropin a pralidoxim by měl být podán co nejdříve po expozici. V závislosti na závažnosti příznaků, okamžitě aplikujte jednu atropin-obsahuje auto-injector, následuje jeden pralidoxim-obsahuje auto-injector. Atropin musí být podáván nejprve, dokud se jeho účinky nezjistí, a teprve poté by měl být pralidoxim podáván. Pokud jsou příznaky nervového činidla stále přítomny po 15 minutách, opakujte injekce. Pokud příznaky přetrvávají po dalších 15 minutách, opakujte injekce potřetí. Pokud po třetí sadě injekcí přetrvávají příznaky, nepodávejte žádné další antidota, ale vyhledejte lékařskou pomoc.
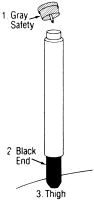
Když, jak je popsáno výše, auto-injector použití je uvedeno, postupuje se takto:
|
 |
VELMI závažný PŘÍPAD — Cyanóza, Respirační Rozpaky, Kóma
Základní opatření by měla zahrnovat odstranění sekretů, udržování průchodnosti dýchacích cest a v případě potřeby, umělá ventilace. Atropin by neměl být používán, dokud není překonána cyanóza, protože atropin produkuje komorové fibrilace v přítomnosti hypoxie. Morfin, teofylin, aminofylin nebo sukcincylcholin jsou kontraindikovány. Je třeba se vyhnout trankvilizérům typu reserpin nebo fenothiazin.
“ Pralidoxim je nejúčinnější, pokud se podává okamžitě po otravě. Obecně je málo dosaženo, pokud je lék podán více než 36 hodin po ukončení expozice. Po požití jedu však může expozice po určitou dobu pokračovat v důsledku pomalé absorpce z dolního střeva a po počátečním zlepšení byly hlášeny fatální relapsy. U těchto pacientů může být užitečné pokračovat v podávání po dobu několika dnů. Pečlivý dohled nad pacientem je indikován po dobu nejméně 48 až 72 hodin. Pokud dojde k dermální expozici, je třeba oděv odstranit a vlasy a pokožku co nejdříve důkladně omýt hydrogenuhličitanem sodným nebo alkoholem. Diazepam může být podáván opatrně, pokud křeče nejsou kontrolovány atropinem.“7
důležité: lékaři a / nebo jiný zdravotnický personál, který pomáhá evakuovaným obětem nervových agens, by se měli vyhnout vystavení kontaminaci oděvem obětí.
jak se Pralidoxim chlorid dodává
Pralidoxim chlorid se dodává ve vodném roztoku předplněném v autoinjektoru (600 mg, 2 mL) pro vojenské použití a pro použití kvalifikovanými civilními záchranáři. Auto-injektory jsou dodávány prostřednictvím Ředitelství Zdravotnického Materiálu, Obrana Nabídky Centra Filadelfie nebo jiné obdobné místní, státní nebo federální agentury.
Když jsou aktivovány, každé auto-vstřikovač dávkuje 600 mg Pralidoxim Chloridu sodného ve 2 mL sterilní roztok obsahující 20 mg/mL benzylalkohol, 11.26 mg/mL glycin ve Vodě pro Injekce, USP. PH se upraví kyselinou chlorovodíkovou. PH je 2,0-3,0 produkt neobsahuje pyrogen.
uchovávejte při teplotě 25°C (77 ° F); exkurze jsou povoleny na 15-30°C (59-86°F).
Chraňte před mrazem.
Meridian Medical Technologies, Inc.
Columbia, MD 21046
Pfizer Společnost
00001976
08/16
Vytištěno v U. S. A.
- Landauer, W.: Cholinomimetickému tetrogens. V. účinek oximů a příbuzných reaktivátorů cholinesterázy, teratologie 15:33 (Únor.) 1977.
- Moller, K. O., Jenson-Holm, J., a Lausen, h. H.: Ugeskr. Laegu.123:501, 1961.
- Namba, T., Nolte, C. T., Jackrel, Jr., and Grob, D.: otrava způsobená organofosfátovými insekticidy. Akutní a chronické projevy, Amer. J.Med. 50: 475 (Duben.) 1971.
- Arena, J. M.: otrava. Toxikologie. Příznak. Léčba, Ede. 4, Springfield, Nemocný., Charles C. Thomas, 1979, s. 133.
- Brachfeld, J., and Zavon, M. R.: intoxikace organickým fosfátem (Fosdrin®). Zpráva o případu a výsledky léčby 2-PAM, Arch. Environ. Zdraví 11: 859,1965.
- Hayes, W. J., Jr.: Toxikologie Pesticidů, Baltimore, Williams & Wilkins Společnosti, 1975, str. 416.
- oddělení léčiv ama: hodnocení léčiv Ama, ed. 4, Chicago, Americká lékařská asociace, 1980, s. 1455.
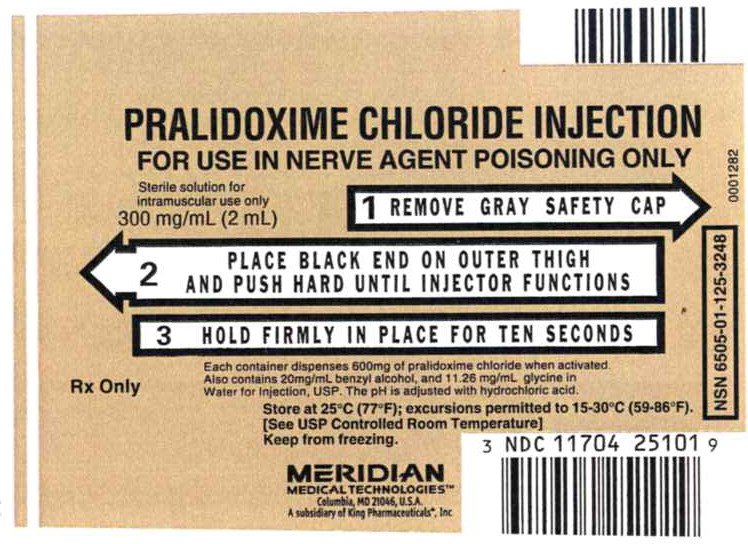
Hlavní Displej – Pralidoxim Chloridu sodného na Injekci 300 mg Label
NDC 11704-107-01
Pralidoxim Chloridu sodného na INJEKCI
PRO POUŽITÍ V NERVOVÉHO plynu POUZE
Sterilní roztok pro intramuskulární použití pouze
300 mg/mL (2 mL)
1 SEJMĚTE ŠEDÝ BEZPEČNOSTNÍ kryt,
2. MÍSTO ČERNÝ KONEC NA VNĚJŠÍ STEHNA A ZATLAČTE, DOKUD INJECTOR FUNKCE,
3 DRŽET PEVNĚ NA MÍSTĚ PRO DESET SEKUND
Každý kontejner dávkuje 600mg Pralidoxim-Chlorid, pokud je aktivován.
také obsahuje 20 mg/mL benzylalkoholu a 11.26 mg / mL glycinu v
voda na injekci, USP. PH se upraví kyselinou chlorovodíkovou.
pouze RX
uchovávejte při teplotě 25°C (77 ° F); exkurze jsou povoleny na 15-30°C (59-86°F).
Chraňte před mrazem.
MERIDIAN MEDICAL TECHNOLIGIESTM
Columbia, MD 21046, USA
A subsidiary of King Pharmaceuticals®, Inc
NDC 11704-251-01
NSN 6505-01-125-3248
| Pralidoxime Chloride Pralidoxime Chloride injection |
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
Labeler – Meridian Medical Technologies, Inc. (167671341)
| Establishment | |||
| Name | Address | ID/FEI | Operations |
| Meridian Medical Technologies, Inc. | 038889234 | MANUFACTURE(11704-251), ANALYSIS(11704-251) | |
| Establishment | |||
| Name | Address | ID/FEI | Operations |
| Meridian Medical Technologies, Inc. | 078808315 | MANUFACTURE(11704-251), LABEL(11704-251), PACK(11704-251) | |
| Establishment | |||
| Name | Address | ID/FEI | Operations |
| Meridian Medical Technologies, Inc. | 167671341 | MANUFACTURE(11704-251), LABEL(11704-251), PACK(11704-251), ANALYSIS(11704-251) | |
Více o pralidoxim
- Nežádoucí Účinky
- Během Těhotenství
- Dávkování Informací
- lékové Interakce
- En Español
- třídy Drog: protilátky
- FDA Upozornění (1)
Spotřebitelské zdroje
- Informace pro Pacienta
- Pralidoxim Injekce (Pokročilé Čtení)
Odborné zdroje
- Předepisování Informace
- Pralidoxim (Profesionální Pacient Poradenství)
Jiných značek Protopam Sodný
Související léčba vodítka
- Cholinesterázy Předávkování
- Otravu Organofosfáty
- Nervového plynu
Medical Disclaimer