Il primo farmaco biologico, l’insulina umanizzata (5,8 kDa), è diventato disponibile nel 1982 in seguito all’avvento delle biotecnologie e ha segnato una nuova era nell’industria farmaceutica. I moderni progressi nella biotecnologia consentono sintesi su larga scala di prodotti biologici in modo più o meno conveniente. Avendo una volta iniziato con grandi peptidi e proteine ricombinanti, i biologici oggi includono una vasta gamma di altre entità, come anticorpi, anticorpi monoclonali e più recentemente, nanobodies e oggetti correlati, recettori solubili, DNA ricombinante, coniugati anticorpo-farmaco (ADC), proteine di fusione, immunoterapeutici e vaccini sintetici.
La “stella nascente” dei farmaci biologici ha catturato l’attenzione crescente dei professionisti farmaceutici e degli analisti del settore, poiché questo paradigma di scoperta di farmaci alternativi rappresenta una sfida commerciale sostanziale per il paradigma di scoperta di farmaci di piccole molecole più tradizionale che definisce l’industria farmaceutica per più di un secolo.
Quindi sorge la domanda: le piccole molecole stanno perdendo “attrattiva” come oggetti di ricerca per la scoperta di farmaci nel mondo moderno dei progressi biologici? Alcuni esperti rimangono ottimisti sul potenziale delle piccole molecole di guidare la corsa nei futuri gasdotti farmaceutici, altri percepiscono che “i soldi stanno cambiando le tasche” e la ricerca sulle piccole molecole sarà sempre più trascurata dagli azionisti e dagli investitori a favore dei biologici.
Per capire dove si sta dirigendo l’industria, iniziamo prima con un po ‘ di statistiche. Per un periodo di 7 anni (2010-2017) U. S. La Food and Drug Administration (FDA) ha approvato un totale di 262 nuove entità molecolari (NME), esclusi diversi agenti di diagnostica per immagini e 1 analogo dell’insulina (ref). Sembra che il 76% di loro sono piccole molecole (199) con solo un quarto essendo biologici. È interessante notare che non vi è alcuna crescita apparente nelle approvazioni NMEs biologiche rispetto alle piccole molecole in quanto entrambe le categorie di terapie sono di tendenza in modo abbastanza simile, come mostrato nello schema seguente. Tuttavia, poiché i biologici hanno un prezzo molto diverso dalle piccole molecole (sono molto più costosi), il quadro è diverso se si guarda alle vendite totali e alla crescita dei ricavi: nel periodo dal 2011 al 2017 i ricavi delle vendite biologiche sono cresciuti del 70% raggiungendo $232 miliardi. La quota del mercato farmaceutico totale che i biologici detengono è aumentata dal 16% nel 2006 fino al 25% nel 2016, senza segni apparenti di rallentamento (ref).
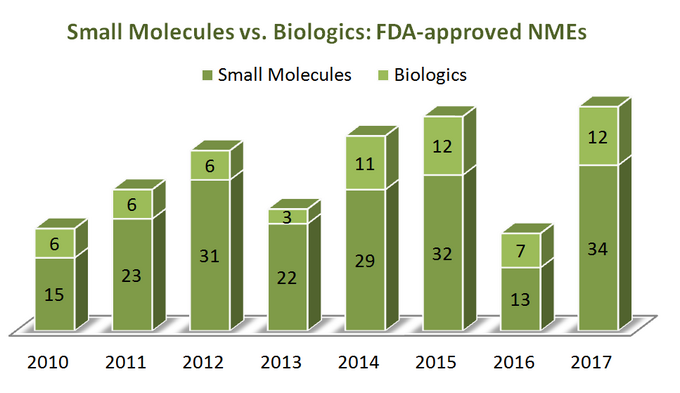
Mentre ci sono vantaggi distintivi dei biologici rispetto alle piccole molecole in diversi modi (ad esempio, la loro profonda selettività), le cose non sono “in bianco e nero” quando si confrontano queste due categorie di terapie con i loro attributi, poiché entrambe hanno pro e contro sostanziali da considerare durante il processo decisionale strategico. Quindi sembra un po ‘deplorevole vedere come numerosi rapporti messo da parte SMS rispetto ai biologici in una ricerca di” freschezza” dei loro punti di vista.
Una tabella seguente riassume alcuni aspetti forti e deboli di entrambe le categorie (ref, ref) illustrando sfide e opportunità disponibili in entrambi i “campi” (nota colori: grigio – nessun vantaggio apparente in nessuno dei due campi; verde-situazione vantaggiosa ;giallo-situazione svantaggiosa):
Piccole Molecole |
Biologics |
|---|---|
|
Proprietà generali |
|
|
a Basso peso molecolare (0,1 – 1 kDa); di solito, chimicamente e termicamente stabile, ampia gamma di polarità. |
Pesi molecolari molto grandi > 1 kDa; generalmente polare, sensibili al calore, facilmente degradati (con l’eccezione di alcune longevo tipi di anticorpi monoclonali) |
|
Selettività, di sicurezza |
|
|
Piuttosto promiscua, di solito si legano ai diversi target siti, il rendering di effetti collaterali o tossicità. Infine, gli sviluppatori biologici hanno avuto un tempo più facile ottenere brevetti perché c’è stato poco o nessun state-of-art nel campo, quando sono stati scoperti i blockbuster attuali. |
Altamente specifico per gli obiettivi, generalmente di tossicità inferiore (con una grande eccezione è quella dell’immunogenicità, che può influenzare seriamente l’efficienza, la sicurezza e la disposizione dei prodotti biologici). |
|
Permeabilità cellulare |
|
|
SMS si legano con bersagli come recettori accoppiati alla proteina G (GPCRs), canali ionici ligandi-gated e recettori tirosin chinasi sul domini extracellulari o intracellulari. Possono accedere a bersagli nelle regioni intracellulari, citosol, nuclei e persino bersagli del SNC, separati dalla stretta barriera emato-encefalica (BBB). |
Una grande percentuale di bersagli farmacologici sono incorporati e quindi inaccessibili ai farmaci biologici. Soprattutto, quando si tratta di sistema nervoso centrale (SNC), la presenza della barriera emato-encefalica è un ostacolo importante sulla strada di qualsiasi molecola più grande di 600 Da che limita fino al 98% di SMS e praticamente tutti i biologici. |
|
Delivery |
|
|
Rientrano in gran parte nella “Regola dei cinque” per l’assorbimento orale, rendendolo adatto per la consegna orale. L’ulteriore permeabilità attraverso l’epitelio intestinale è principalmente mediata da una combinazione di diffusione passiva e trasporto paracellulare. |
L’instabilità intrinseca e le masse molecolari elevate rendono quasi tutti i biologici oralmente inattivi. Per lo più, consegna invasiva, o tecnologie alternative non invasive in corso. |
|
Distribuzione |
|
|
Gli SMS vengono distribuiti tramite la circolazione sanguigna, consentendo di raggiungere rapidamente le concentrazioni di prelievo. |
Per molecole più grandi (ad esempio > 10 kDa) un sistema linfatico più lento (di 100-500 volte) diventa dominante nel processo di distribuzione. I più grandi biologici distribuiscono via sia il sangue che i sistemi linfatici che muovono il trasporto convettivo, l’endocitosi mediata dal recettore, la fagocitosi e la pinocitosi. Il risultato di questa situazione è che i biologici più grandi hanno emivite più lunghe, volumi limitati di distribuzione e hanno bisogno di più tempo per raggiungere le concentrazioni di picco, rispetto agli SMS. |
|
Disposition (metabolism) |
|
|
La maggior parte degli SMS viene smaltita da organi non mirati-tramite metabolismi citocromi o non citocromi, filtrazione renale o escrezione fecale. |
I biologici hanno interazioni più strette con gli obiettivi, quindi le loro disposizioni sono direttamente influenzate dal loro legame (disposizione del farmaco mediata dal recettore), comprese le distanze dei biologici dalle proteasi e dalla peptidasi. |
|
interazioni farmacologiche |
|
|
SMs sono inclini a interazioni farmacologiche che possono verificarsi a causa della presenza concomitante di farmaci che influenzano il loro trasporto, il metabolismo, il trasporto o l’eliminazione dei percorsi. |
I biologici sono meno inclini alle interazioni farmacologiche tradizionali poiché subiscono il metabolismo e l’eliminazione come substrati endogeni. Tuttavia, ci sono cambiamenti documentati cytokine-mediati nella droga che metabolizza gli enzimi, quindi le interazioni farmaco-biologiche devono essere valutate nel caso in cui la droga possa influenzare l’espressione degli enzimi metabolici. |
|
Aspetti aziendali |
|
|
Prezzi bassi per i farmaci SM. |
In genere, prezzi molto alti per i trattamenti biologici. Questo è considerato come uno dei motivi biologici sembrano essere offrendo migliori rendimenti economici complessivi, rispetto a SMS. |
|
Alto tasso di attrito (lo studio del 2009 del gruppo KMR ha dimostrato che solo il 7,1% degli SMS che entrano nei test preclinici ha raggiunto il mercato). |
Tasso di logoramento relativamente basso (lo stesso studio del gruppo KMR ha rivelato che il 24,4% dei biologici in fase preclinica è sopravvissuto fino allo stadio di mercato). |
|
Severe competition from chemical generics after patents expiration. |
Biologics developers face less severe competition from biosimilars, after patents expiration. |
|
Simpler drug discovery/development process. |
More expensive and complex drug discovery and development process, compared to biologics. |
Considerando il confronto di cui sopra, è evidente che i prodotti biologici non sono una “pallottola magica” e l’industria non sarà dominato da prodotti biologici nel prossimo futuro, piuttosto, un equilibrio competitivo sarà mantenuta tra le molecole piccole, di prodotti biologici e forme ibride di terapie, come Adc — con locale dominazione di ogni modulo più adatto aree terapeutiche, i casi d’uso etc.
Inoltre, sotto è un elenco di più l’industria dei driver che stanno giocando sul lato di piccole molecole e potrebbe influenzare il bilanciamento dei poteri, nel totale del mercato farmaceutico in favore di chimica punti di partenza:
L’aumento di intelligenza artificiale (AI) nella scoperta della droga
a Seguito di innovazioni nel profondo algoritmi di apprendimento (2012) e, più recentemente, la creazione di generativa contraddittorio reti (GANs), in grado di eccellere in una serie di attività di ricerca, l’interesse nei vari AI technologies è salito alle stelle in praticamente ogni settore. Molti strumenti AI-powered è diventato rapidamente mainstream commerciale, come chatbots, assistenti personali, autopiloti ecc.– che è una prova del mondo reale del concetto di fattibilità AI.
Drug discovery non è un’eccezione a questa “tendenza guidata dall’IA”, e il numero di start-up che cercano di applicare l’IA per aumentare la scoperta di farmaci in modi diversi è cresciuto sostanzialmente in pochi anni, avendo raggiunto oltre un centinaio di aziende attive fino ad oggi (ecco un elenco di alcune di esse).
È interessante notare che la maggior parte delle start-up AI-driven si concentra sulla scoperta di piccole molecole di droga, piuttosto che biologici, che è, probabilmente, non sorprendente. Storicamente, anche i metodi computazionali non-AI (cheminformatica) sono stati utilizzati principalmente per la terapia a piccole molecole a causa delle loro strutture molecolari e modelli di interazione sostanzialmente più semplici.
Il diagramma seguente mostra una statistica stimata per 61 start-up di scoperta di farmaci attivamente commercializzati che sviluppano o applicano strumenti AI specializzati nel loro flusso di lavoro di ricerca. Come si può vedere, la metà di tutte le aziende (51%, 31 startup) è focalizzata su piccole molecole, mentre solo il 23% (14 startup) è coinvolto nella scoperta/sviluppo di farmaci biologici (anticorpi, vaccini ecc.). La sproporzione verso le piccole molecole è anche ben illustrata dalla quantità di finanziamenti VC raccolti collettivamente da 61 startup guidate dall’IA (solo round divulgati pubblicamente)-dove 770 milioni sono stati investiti in quelle società coinvolte in piccole molecole e solo poco più di 200 milioni è stato assegnato per start-up incentrate sui biologici-come mostrato di seguito.
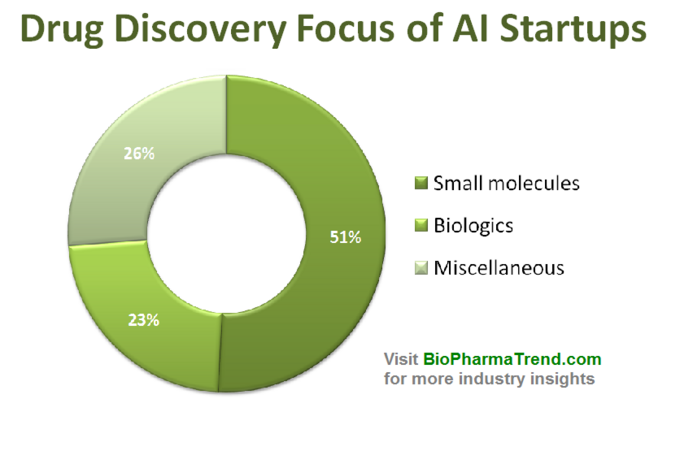
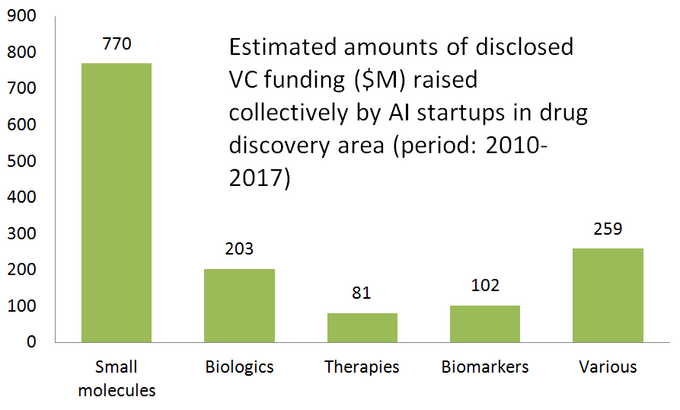
Questa situazione suggerisce che i recenti progressi negli algoritmi di IA e una tendenza ad applicare l’apprendimento automatico per la ricerca farmaceutica in fase iniziale tendono a guidare una maggiore crescita nella scoperta di farmaci a piccole molecole, rispetto alla scoperta biologica least almeno per ora. Ciò potrebbe portare a maggiori investimenti futuri in progetti focalizzati su piccole molecole supportati da tecnologie guidate dall’IA.
Raggiungere obiettivi “non riparabili”
Obiettivi importanti come, ad esempio, le interazioni proteina-proteina (PPI), sono tradizionalmente dominati dai biologici (mAbs) come potenziali attori, mentre le piccole molecole erano state a lungo considerate inadatte in questo caso a causa delle loro piccole dimensioni.
Con i progressi della farmacogenomica, questa situazione può cambiare piuttosto rapidamente dopo le approvazioni maraviroc (514 Da) e tirofiban (441 Da). È stato rivelato computazionalmente che gli SMS possono effettivamente avere affinità relativamente elevate con specifiche interfacce di proteine e, cosa importante, possono modulare le “regioni proteiche intrinsecamente disordinate” legate a un insieme di malattie complesse dei sistemi. Ecco un interessante cover up di questo argomento che riassume alcune delle importanti intuizioni sui macchinari PPI ottenuti negli ultimi decenni.
Un’altra area in rapida crescita per la scoperta di farmaci a piccole molecole sta prendendo di mira l’acido ribonucleico (RNA). Questo argomento è stato elencato in ” Top 7 Trends In Pharmaceutical Research In 2018″, e c’è stata anche una revisione dettagliata dell’argomento in Biologia chimica cellulare e una bella copertura industriale in C&EN.
Un’altra nuova idea per scatenare il potere delle piccole molecole è stata discussa in un recente articolo”I degradatori proteici mirati stanno ridefinendo il modo in cui le piccole molecole appaiono e agiscono”pubblicato in C&EN nel 2018. La strategia qui è quella di sviluppare piccole molecole bifunzionali in grado di indirizzare una proteina mirata del tutto al proteasoma, la macchina di rimozione dei rifiuti della cellula, invece di inibire l’azione della proteina come in un approccio “tradizionale”.
Superare le limitazioni delle tecnologie di screening
Un sacco di potenziale di ricerca di piccole molecole non è stato ancora realizzato a causa di varie limitazioni tecnologiche degli approcci di screening utilizzati per identificare i punti di partenza nei programmi di scoperta di farmaci.
Un esempio è l’approccio di screening fenotipico, che sta vivendo una rinascita al giorno d’oggi a causa di diversi progressi tecnologici, tra cui la crescente capacità di sviluppare modelli cellulari fisiologicamente rilevanti, letture e sofisticate tecnologie di rilevamento che aiutano a rivelare i meccanismi d’azione (MoA) in modo più efficiente, riducendo al minimo l’incertezza. D’altra parte, l’implementazione di tecniche di profilazione su larga scala e metodi computazionali offre un nuovo livello di analisi dei sistemi e comprensione dei fenotipi di piccole molecole.
Un altro paradigma di screening promettente è tramite l’utilizzo di librerie codificate dal DNA (DELS). Grazie alla sua disposizione unica, la tecnologia DEL fornisce un modo adatto per testare centinaia di milioni e persino miliardi di nuove molecole in programmi di scoperta di farmaci basati su target. Sebbene questa tecnologia non sia priva di sfide (ad esempio limitazioni della chimica compatibile con il DNA, incertezza con i colpi di screening, ecc.), l’area sta crescendo rapidamente ed è persino considerata “rivoluzionaria” per la scoperta di farmaci di piccole molecole.
il Superamento synthesizability barriera
Una delle pietre d’inciampo della fase precoce piccola molecola scoperta della droga è una limitazione del sinteticamente accessibile spazio chimico — mentre un sacco di promettente chimica idee possono essere generati informaticamente, o altrimenti, c’è sempre il rischio che la sintesi tutta la serie di composti per convalidare tali idee sarebbe costoso, o addirittura irrealizzabile.
Recenti progressi in questo settore sono stati fatti, ancora una volta, utilizzando software basato su AI che offre prestazioni di pianificazione di sintesi a livello umano. Ad esempio, BenevolentAI ha recentemente pubblicato un articolo su Nature, descrivendo come hanno usato reti neurali profonde in combinazione con moderni algoritmi di ricerca ad albero per pianificare la sintesi di nuove molecole con notevole tasso di successo e velocità.
Diverse cover up interessanti con ricchi commenti sono stati pubblicati qui e qui da Derek Lowe fornendo un po ‘ più di comprensione in questa affascinante area della chimica organica e medicinale.
Una strategia più empirica è stata sviluppata da un produttore chimico Enamine, che è noto come Spazio chimico reale, e attualmente comprende oltre 3.8 miliardi di molecole sinteticamente accessibili e ricercabili per l’esplorazione hit e altri compiti di chimica medicinale. Il concetto si riduce all’applicazione di una serie di percorsi chimici convalidati internamente (oltre 100 reazioni) a un ampio pool di blocchi chimici disponibili in magazzino (oltre 100 mila composti)-con l’obiettivo di combinarli in modo combinatorio per produrre una cascata di molecole più grandi “simili al piombo” o “simili a farmaci”. Una volta raggiunto un certo grado di riproducibilità e resa in un insieme sufficientemente ampio di esperimenti (almeno l ‘ 80%), viene effettuata un’ulteriore enumerazione computazionale per costruire uno spazio chimico più ampio basato sui casi convalidati sperimentalmente.
New R& D mercati e ruoli per piccole molecole
Tutto sommato, si può trascurare o fraintendere le dimensioni e il potenziale di crescita delle pipeline di piccole molecole, come è stato menzionato durante una tavola rotonda a Interphex. Attualmente, circa 8000 piccole molecole sono attive in R&D, una crescita del 25% negli ultimi due anni. I fattori di crescita sopra elencati possono portare a un’ulteriore accelerazione della crescita in questo settore.
È anche importante notare che i farmaci a piccole molecole potrebbero svolgere un ruolo importante in alcuni farmaci di prossima generazione, rendendoli dipendenti da pipeline di piccole molecole. Ad esempio, nel caso della terapia con cellule staminali, piccole molecole possono innescare reazioni terapeutiche.
Come è stato evidenziato durante CPhI North America da Jeffrey Shumway di MilliporeSigma, i prodotti a piccole molecole tendono a diventare più complessi, alterando il loro ruolo nell’industria farmaceutica (bio).
Infine, l’area futura per le piccole molecole sono i coniugati anticorpo-farmaco e gli oggetti correlati, che sono emersi come una promettente classe di terapie a causa della naturale convergenza di due paradigmi di scoperta dei farmaci e di molteplici tendenze tecnologiche.
Disclaimer: Le informazioni sono solo per la consapevolezza generale, e non è un legale/finanziario/stock trading/consulenza medica di qualsiasi tipo. Lo leggi a tuo piacimento e qualsiasi utilizzo di queste informazioni è a tuo rischio. E ‘ vostra responsabilità di valutare l’utilità e la sicurezza delle informazioni in questo post, e Internet in generale, e come si applica alla propria situazione e quindi consultare gli esperti competenti per consulenza professionale, se necessario.
Argomenti: Tendenze del settore