
Sau(ラリー)Lee、Ph.D.、テストと研究のオフィスの副ディレクター、および新興技術チーム、医薬品品質、CDERのオフィスの椅子
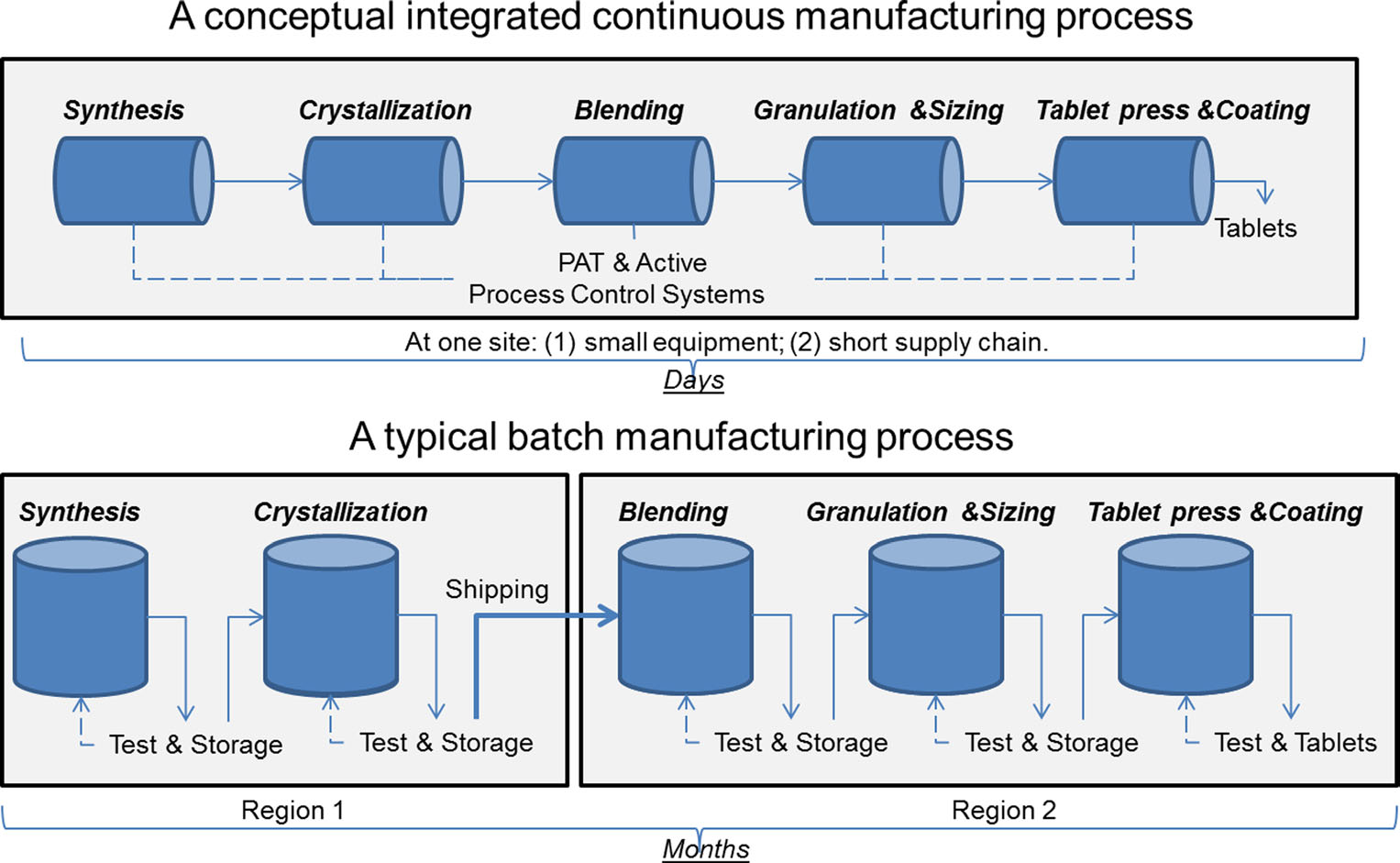 連続製造とバッチ製造の比較。 画像提供:食べログのソウ-リーさん(元画像)。 J.Pharm Innov(2015)10:191-199.
連続製造とバッチ製造の比較。 画像提供:食べログのソウ-リーさん(元画像)。 J.Pharm Innov(2015)10:191-199.50年以上にわたり、医薬品は”バッチ製造”として知られている方法を使用して製造されてきました。 しかし、製造技術の最近の進歩は、バッチ製造から連続製造として知られているより速く、より効率的なプロセスに移行することを検討する製薬業界 FDAは、製品の品質を向上させ、薬物不足やリコールの根本的な原因の多くに対処するために、継続的な製造を含む新興技術の製薬業界の実装を容易にす
バッチ対連続製造
バッチ製造には、複数の個別のステップが含まれます。 プロセスの各ステップの後で、生産は普通停止します従ってサンプルは質のためにオフラインでテストすることができます。 時々ステップ間のこれらの「保持時間」の間に、材料は容器で貯えられるか、または製造工程を完了するために世界中で他の設備に出荷されるかもしれ これにより、処理時間に数週間または数ヶ月が追加される可能性があります。 環境に敏感であるある有効成分のために、それはまた低下の危険をもたらすかもしれません。 さらに、特定の医薬品の需要が急増した場合、生産量の増加にはより大きな設備が必要になる可能性があります。 このような機器のスケールアップには、より多くの物理的なスペース、より大きなフットプリント、そしてより多くの時間とお金が必要です。対照的に、連続製造を使用して製造された医薬品は、同じ施設内でノンストップで移動され、ステップ間の保持時間がなくなります。 材料は十分に統合された部品の一貫作業を通して与えられる。 この方法は、時間を節約し、人的ミスの可能性を低減し、市場の変化により機敏に対応することができます。 より高い需要を考慮するためには、連続的な製造業は薬剤の不足の可能性を減らすかもしれないより長い一定期間の間動くことができます。
製造の両方のタイプは、同じ品質管理基準の対象となりますが、監視は連続製造施設で自動化され、バッチ製造よりも頻繁になる傾向があります。 すべての技術と同様に、連続製造装置は消耗を経験することができますが、自動監視は障害が発生するずっと前に問題を検出することができます。 このような監視は、機器の平均寿命を予測するのにも役立ち、より積極的なメンテナンスにつながります。最後に、継続的な製造により、より柔軟な追跡と追跡が可能になり、製品の故障が発生した場合の利点になります。 たとえば、バッチ製造では、薬剤の特定の量(またはバッチ)は、それを製造した装置のサイズによって定義されます。 連続的な製造業では、量(かバッチ)はタイムスタンプ、作り出される薬剤の量、または未加工入力材料の量によって描写することができる。 これらの追跡方法は製造業者が不足のより少ない無駄そしてより少ないチャンスをもたらすプロセス失敗の場合に不完全な材料の少量を隔離す
挑戦的だが価値のある移行
化学産業や石油化学産業など、いくつかの産業はすでに製造の進化を遂げており、効率的な連続技術を使用して製品を安全に製造しています。 しかし、製薬業界にとって、継続的な製造への移行はいくつかの理由からまだ初期段階にあります。 第一に、このような移行のための起動コストが高くなる可能性があります。 古いバッチ装置を引退し、新しい技術を購入し、それを使用する方法についてのスタッフを訓練し、業界インフラを刷新することは高価であり、製薬メーカーからの深刻なコミットメントを必要とする。 それでも、経済分析は、潜在的な大幅な長期的な節約を示しています。 さらに、一部の技術はまだ商業的に実行可能である前に成熟する必要があります。 生物学的製品などの特定の種類の薬物については、連続的な製造によってそれらを製造する技術はまだ存在しない可能性がある。 これらの課題やその他の課題に対処するための研究が進行中です。 さらに、製薬会社は、新しい製造技術が使用されたときに製品の承認を遅らせる可能性のある規制上の不確実性を認識しています。
業界が切り替えを行う方法を検討しているように、FDAは移行を容易にするためのリソースと情報を提供しています。 たとえば、米国保健福祉省のプログラムであるBiomedical Advanced Research And Development Authorityと提携して、この分野の研究に資金を提供し、支援しています。 また、レビュースタッフを訓練し、継続的な製造に関連するリスク領域に関する内部調査を実施しているため、関連技術をよりよく評価することがで
私はCDERの医薬品品質オフィスの新興技術プログラムの下で学際的なチームをリードしています。 このプログラムは、医薬品不足やリコールの根本的な原因に取り組むために、業界が製品の品質を向上させ、業界を近代化するための革新的な技術を実 新興技術プログラムは、継続的な製造技術だけでなく、3D印刷、新規剤形、新規コンテナシステムなどの他の進歩にも対応しています。 このプログラムの下で、私たちは新しい技術を開発する過程の早い段階で業界と関わり、将来のアプリケーションの一部となる可能性のある予測された規制上または科学上の問題について議論します。
多くの企業は、継続的な製造への関心に関する新興技術プログラムに適用されています。 FDAの文書”Advancement of Emerging Technology Applications to Modernize The Pharmaceutical Manufacturing Base Guidance for Industry”は、開発プロセスの早い段階で代理店と協力する方法についての情報とアドバイスを提供しています。
FDAのVoiceブログで医薬品製造を近代化するためのFDAの取り組みについての詳細をお読みください。