ほぼすべてのFe–Sタンパク質では、Fe中心は四面体であり、末端リガンドはシステイニル残基からのチオラート硫黄中心である。 硫化物基は二配位または三配位のいずれかである。 これらの特徴を持つ三つの異なる種類のFe–Sクラスタが最も一般的である。
2fe–2S clustersEdit

最も単純な多金属系、クラスターは、二つの硫化物イオンで架橋され、四つのシステイニル配位子(fe2s2フェレドキシンでは)または二つのシステインと二つのヒスチジン(リースケタンパク質では)によって。 酸化された蛋白質は二つのFe3+イオンを含んでいますが、還元された蛋白質は一つのFe3+と一つのFe2+イオンを含んでいます。 これらの種は、(FeIII)2とFeIIIFeIIの二つの酸化状態で存在する。 CDGSH鉄硫黄ドメインはまた、2fe-2Sクラスターに関連付けられています。
4fe–4Sクラスター編集
共通のモチーフは、キューバン型クラスターの頂点に配置された四つの鉄イオンと四つの硫化イオンを特徴とする。 Fe中心は、典型的にはさらにシステイニル配位子によって配位されている。 電子移動タンパク質(フェレドキシン)は、さらに低電位(細菌型)と高電位(HiPIP)フェレドキシンに細分することができる。 低電位および高電位フェレドキシンは、以下の酸化還元スキームによって関連している:

いくつかの4fe–4Sクラスターは基質に結合し、したがって酵素補因子として分類される。 アコニターゼでは、Fe-Sクラスターはチオラート配位子を欠く1つのFe中心でアコニチン酸と結合する。 クラスターは酸化還元を受けませんが、クエン酸塩をイソクエン酸塩に変換するルイス酸触媒として機能します。 ラジカルSAM酵素では、クラスターが結合し、多くの生合成に関与しているラジカルを生成するためにS-アデノシルメチオニンを減少させます。
3fe–4Sクラスターエディット
タンパク質は、より一般的なコアよりも少ない鉄を特徴とする中心を含むことも知られている。 3つの硫化物イオンはそれぞれ2つの鉄イオンを橋渡しし、4つ目の硫化物は3つの鉄イオンを橋渡しする。 それらの正式な酸化状態は、+(すべての-Fe3+形態)から2-(すべての−Fe2+形態)まで変化し得る。 多くの鉄–硫黄タンパク質では、クラスターは酸化と一つの鉄イオンの損失によって可逆的にクラスターに変換することができます。 例えば、aconitaseの不活性形態はFe2+およびreductantの付加によって所有し、活動化させます。
他のFe–Sクラスター編集
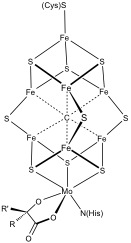
より複雑な多金属系が一般的です。 例としては、ニトロゲナーゼにおける8feと7feクラスターの両方が挙げられる。 一酸化炭素デヒドロゲナーゼと–ヒドロゲナーゼはまた、異常なFe-Sクラスターを特徴とする。 特別な6システイン配位クラスターは、酸素耐性膜結合ヒドロゲナーゼで発見されました。