生物油は、分子構造および特性において石油(”通常の”ディーゼル燃料)

一般的な石油ディーゼル燃料は、平均化学式C12H23(以下に示す)を持つ単純な炭化水素の混合物であるが、コンポーネントは約以下の範囲である可能性がある。ることができる。 対照的に、生物学的油は、以下に示すグリセリルtrilinoleateのような”トリグリセリド”(”エステル”として分類される)である:
| C12H23、ドデカン | トリグリセリド:グリセリルトリリノール酸グリセリル |
その大きなサイズとその結果として大きな分子間魅力のために、生物油の粘度は、一般的に従来のディーゼルエンジンで使用するには高すぎます。 生物的オイルはまた石油のディーゼルよりsootier炎と少しより少し容易に、そして燃える。 生物学的油は、粘度を低下させるために予熱されている場合、従来のディーゼルエンジンで使用することができるが、エンジンが温まるまで補助電気ヒータを必要とする。 これらのresonsのために、bilogicalオイルはバイオディーゼルとして使用のために処理を要求する。
生物油は、以下に示す原子結合を有する有機化合物の一種であるエステルである。
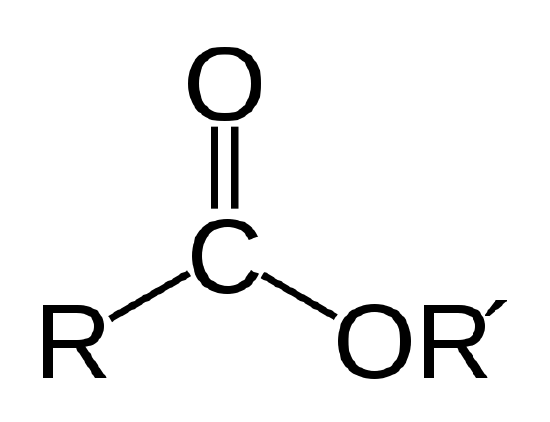 エステルリンケージ。 RおよびR’は、炭素原子および水素原子の鎖を表す。 実施例1におけるステアリン酸メチルのR=-CH3およびR’=-C18H35O2 |
グリセロール |
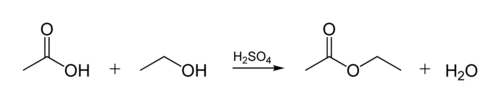
生物油中のエステル結合は、グリセロール分子が有機酸と反応するときに生成される。 グリセロールの分子に3つの炭素原子の鎖が、それの-OH(アルコール)グループとのそれぞれあります。 下の図は、有機アルコールが有機酸とどのように反応するかを示しています。 有機化学者は分子構造を省略しています-図中の「ジグザグ」の線は、それぞれの「ジグザグ」または「ジグザグ」にC原子を有する炭素鎖を表しています。 それぞれの炭素は4つの結合を持ち、4つ未満が示されている場合、それらはH原子に移動すると仮定されます。 したがって、アルコールはC2H5OH(エタノール)であり、酸は酢酸(またはエタン酸、CH3COOH)である:

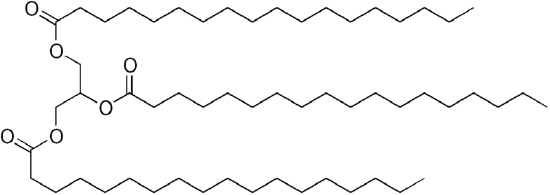
グリセロールは3-oh基を有するので、3つの長鎖有機”脂肪酸”が結合してかさばる”トリグリセリド”を作る。
しかし、エステルはアルコールや酸から作ることができるのと同じくらい簡単に、アルコールや酸を切り替えることができます。 NaOHのような強塩基触媒の存在下では、トリグリセリドは、グリセロール”骨格”を置き換えるメタノール(CH3OH)のような3つの小アルコール分子と反応し、低分子量の3つの別々のエステルを作ることができる
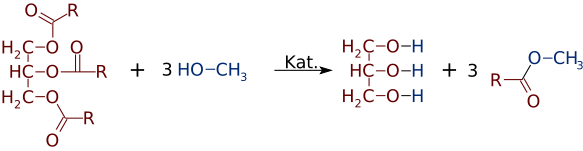
かなり頻繁に二つ以上の生成物の混合物が形成される。 例えば、植物油がメタノールと反応するとき、酸のうちの1つまたは2つだけがグリセリンから置換され、1つまたは2つのFameのみを生成する。
C3H5(C18H35O2)3+NaOH+2CH3OH→C3H5(C18H35O2)2(OH)+2C17H35COOCH3C3H5(C18H35O2)3+NaOH+1CH3OH→C3H5(C18H35O2)(OH)2+1C17H35COOCH3C3H5(C18H35O2)3+naoh+3CH3OH→C3H5(OH)3+3C17H35COOCH3
通常、大量のメタノールと水酸化ナトリウムが添加されるので、反応はFAMEの最大量を生成する。
しかし、エステル交換反応の場合、反応物のどれも完全に消費されないにもかかわらず、生成物の量のさらなる増加は起こらない。
しかし、生成物の量のさらなる増加は起こらない。
私たちは、そのような反応は完了しないと言います。 生成物の混合物が生成されるか、または反応が完了しない場合、反応の有効性は、通常、所望の生成物の収率パーセントの観点から評価される。 理論的収率は、すべての制限試薬が生成物に変換されると仮定することによって計算される。 実験的に決定された生成物の質量を理論収率と比較し、パーセンテージとして表す:

例1 100.0g C3h5(C18H35O2)3ガスと15.0g CH3OHを55℃でNaOH触媒と混合すると、90.96g C17h35COOCH3ステアリン酸メチルバイオディーゼルを形成する。 歩留まり率を計算します。
溶液NH3の理論的収率を計算する必要があり、これを行うには、最初にN2またはH2が制限試薬であるかどうかを発見する必要があります。
溶液NH3の理論的収率を計算する必要があります。 平衡式の場合
C3H5(C18H35O2)3+NaOH+3CH3OH→C3H5(OH)3+3C17H35COOCH3ステアリン+水酸化ナトリウム+3CH3OH→グリセロール+3ステアリン酸メチル
反応物の化学量論比は



 よりも小さいため、Ch3ohが過剰になります。 ステアリンは制限試薬です。 したがって、0.1122molのステアリンと0.3366molのCH3OH(0ではなく)を使用する必要があります。4682 mol CH3OH) to calculate the theoretical yield of C17H35COOCH3 (methyl stearate). We then have
よりも小さいため、Ch3ohが過剰になります。 ステアリンは制限試薬です。 したがって、0.1122molのステアリンと0.3366molのCH3OH(0ではなく)を使用する必要があります。4682 mol CH3OH) to calculate the theoretical yield of C17H35COOCH3 (methyl stearate). We then have so that
so that We can organize these calculations in a table:
We can organize these calculations in a table:
| C3H5(C18H35O2)3(s) | + 3 CH3OH (l) | → 1 C3H5(OH)3 (l) | + 3 C18H35O2)3CH3(s) | ||
|---|---|---|---|---|---|
| m, g | 100.0 g | 15.00 g | 90.96 g | ||
| M, g/mol | 891.5 | 32.04 | 298.5 | 92.1 | |
| n present, mol | 0.1122 mol | 0.4682 mol | |||
| n actual, mol | 0.1122 | 0.3366 | 0.1122 | 0.3366 | |
| m actual, mass | 100.0 | 10.78 | 10.33 | 100.47 |
The percent yield is then
Transesterification is a classic example of a reaction which does not go to completion.