istnieją eksperymentalne metody wykrywania niesparowanych elektronów. Jedną z cech niesparowanych elektronów w materiałach jest interakcja z polem magnetycznym. Ta interakcja może być wykorzystana do dostarczenia informacji o związkach zawierających niesparowane elektrony.
elektronowy rezonans paramagnetyczny
elektronowy rezonans paramagnetyczny (EPR) lub elektronowy rezonans spinowy (ESR) jest metodą spektroskopową. Polega ona na energetycznym rozdzieleniu dwóch stanów spinowych, które występują tylko w obecności pola magnetycznego.
EPR jest bardzo blisko spokrewniony z innym powszechnym rodzajem spektroskopii rezonansu spinowego, NMR.
Spin jest własnością kwantową, która nie ma prawdziwej analogii, która miałaby dla nas sens na poziomie makroskopowym. Wiemy jednak, że spin ma związane z nim właściwości magnetyczne. Elektron może mieć jedną z dwóch wartości dla tych właściwości magnetycznych. Istnieją różne etykiety podane do tych wartości: czasami ” w górę „i” w dół”, czasami, +1/2 i -1/2. Jednakże, niezależnie od tego, jaką wartość spinu posiada elektron, nie ma żadnej różnicy pod względem energetycznym.
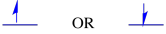
dwa możliwe Stany spinu są takie same energetycznie-chyba że występuje pole magnetyczne. Gdy taka sytuacja się pojawi, następuje energetyczny rozdział między tymi dwoma stanami.
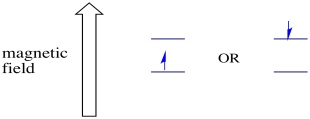
w obecności pola magnetycznego dwa stany spinu dzielą się na dwa różne poziomy energii. Wielkość separacji między poziomami energii zależy od wielkości pola magnetycznego. Im silniejsze pole magnetyczne, tym większa separacja.
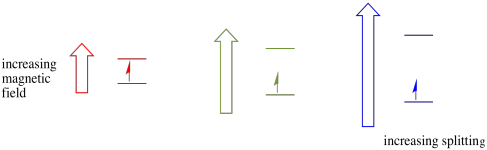
ten przypadek dotyczy tylko niesparowanych obrotów. Pamiętaj, niesparowane spiny oddziałują z polem magnetycznym. Jeśli wszystko jest sparowane, nic się nie dzieje. To bardzo przydatne, ponieważ daje nam sposób na wykrycie niesparowanych elektronów.
elektron w jednym stanie spinowym może być wzbudzony do drugiego przez absorbcję fotonu. Alternatywnie, elektron w wyższym stanie może spaść do niższego, jeśli uwolni Foton.
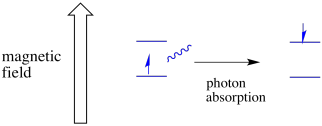
aby to się stało, energia fotonu musi dokładnie odpowiadać różnicy energii między Stanami. Ta zasada Złotowłosej nazywana jest stanem rezonansowym. Ilość dostarczanej energii, aby przejść z jednego poziomu energii do następnego musi być w sam raz. Za mało energii i elektron nie przeżyje. Za dużo energii i elektron też nie da rady. Czeka na odpowiedni Foton.
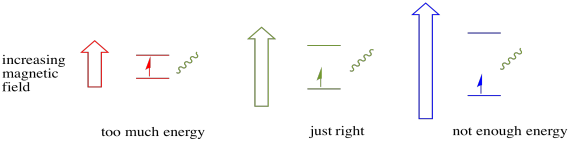
ile energii ma Foton? Pamiętaj o swoim związku Plancka z Einsteinem. Opisuje energię fotonu:
\(e=h \nu \)
E jest energią fotonu, H jest stałą Plancka (6,625 x 10-34 Js), a ν jest częstotliwością fotonu (wygląda jak Rzymska vee, ale to grecka litera, nu).
alternatywnie, ze względu na związek między długością fali a częstotliwością:
\(e= \frac{hc}{\lambda}\)
nowe wielkości to c, Prędkość światła (3,0 x 108 m s-1) i λ, długość fali fotonu.
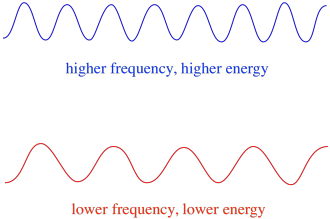
tak więc ogólnie różne długości fal światła dostarczają różne ilości energii. Światło niebieskie o długości fali bliskiej 475 nm ma więcej energii niż światło czerwone o długości fali bliskiej 700 nm.
w EPR ogólnym zakresem promieniowania elektromagnetycznego lub ogólnym rodzajem fotonu jest promieniowanie mikrofalowe. Częstotliwość tych fotonów wynosi około 9 lub 10 GHz. (Inny rodzaj spektroskopii, spektroskopia rotacyjna, mierzy również absorbancję mikrofal. Zwykle wykorzystuje nieco wyższe częstotliwości mikrofal. Spektroskopia rotacyjna daje informacje strukturalne lub wiązania o cząsteczkach w fazie gazowej.)
w zależności od środowiska niesparowanego elektronu, może on być bardziej podatny lub mniej podatny na działanie zewnętrznego pola magnetycznego. Oznacza to, że podział energii między dwoma stanami spinowymi będzie się różnić w zależności od cząsteczki. W rezultacie różne cząsteczki w tym samym polu magnetycznym absorbowałyby różne długości fal promieniowania mikrofalowego.
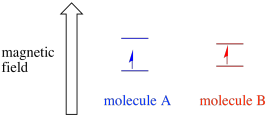
Zwykle spektrometr EPR jest zaprojektowany tak, aby dostarczał do próbki stałą długość fali promieniowania mikrofalowego. Pole magnetyczne jest regulowane, a przyrząd mierzy siłę pola potrzebną do absorpcji fotonów. Widmo EPR pokazuje absorbancję jako funkcję natężenia pola magnetycznego.
w sposobie wyświetlania widm EPR jest coś nieco innego. Jest wyświetlany jako pochodna wykresu pokazanego powyżej. Wynika to ze sposobu, w jaki przyrząd mierzy zmianę absorbancji, gdy zmienia pole magnetyczne; tj. mierzy d(absorbancja)/d(pole magnetyczne). To nachylenie poprzedniej działki.
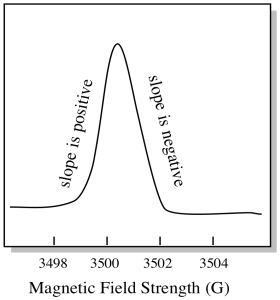
w rezultacie widmo EPR wygląda bardziej tak. Część powyżej linii podstawowej odzwierciedla dodatnie nachylenie na poprzednim wykresie. Część poniżej wartości wyjściowej odzwierciedla ujemne nachylenie na poprzednim wykresie.
Natężenie pola magnetycznego nie jest zazwyczaj wartością podawaną dla pozycji szczytowej. Zamiast tego podaje się coś, co nazywa się wartością G. Wartość g wynika z równania dla efektu Zeemana (wpływ pola magnetycznego na podział między poziomami energii spinu). Zależność ta jest następująca:
\(\Delta e = g \beta b\)
, w której ΔE jest różnicą energii między Stanami spinu, G jest wartością g, stałą proporcjonalności, która zależy od tego, jak podatny jest elektron na działanie pola magnetycznego, β jest magnesem Bohra (9,274 x 10-24 J T-1), A B jest przyłożonym polem magnetycznym.
oznacza to, że dla Absorpcji fotonów,
\(h \nu = g \beta B\)
i tak
\(g = \frac{ h \nu}{\beta B}\)
pamiętaj, h i β są tylko stałymi. Oznacza to, że g jest miarą stosunku fotonu pochłoniętego do użytego pola magnetycznego. To krok standaryzacyjny. Jeśli ludzie mają instrumenty, które używają nieco różnych długości fal promieniowania mikrofalowego, to pola magnetyczne, które mierzą dla tych samych próbek, nie zgadzają się. Jeśli wszyscy mierzą stosunek długości fali do natężenia pola, to wszystko powinno się wyrównać. Wartość g jest powtarzalną miarą środowiska elektronu, który powinien być taki sam z jednego laboratorium do drugiego.
podobną praktykę stosuje się w spektroskopii NMR, z podobnych powodów. Kiedy zgłaszamy zmianę chemiczną w ppm zamiast Hz, korygujemy siłę pola magnetycznego w instrumencie, którego używamy. W przeciwnym razie ta sama próbka dałaby dwa różne przesunięcia na dwóch różnych instrumentach.
sprzężenie w EPR
sprzężenie jest zjawiskiem, w którym pola magnetyczne oddziałują ze sobą. W EPR sprzężenie powstaje z powodu wpływu pobliskich jąder na obserwowany elektron.
na przykład, możesz już wiedzieć, że jądro atomu wodoru ma niesparowany spin. To podstawa spektroskopii 1H NMR. Jeśli jądro ma niesparowany spin, to ma związane z nim pole magnetyczne. Ponieważ jądro wodoru może mieć albo wartość spinu, +1/2 albo -1/2, to ma dwa możliwe pola magnetyczne z nim związane.
pobliski elektron, umieszczony w zewnętrznym polu magnetycznym, może teraz znajdować się w jednej z dwóch różnych sytuacji. Albo sąsiadujący proton dodaje trochę do pola magnetycznego, albo odejmuje trochę od pola zewnętrznego.
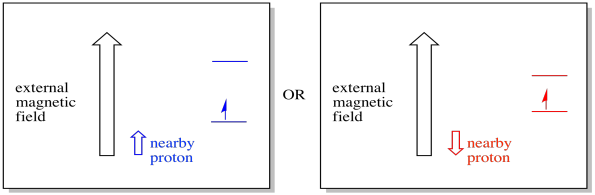
w rezultacie elektron może doświadczać dwóch różnych pól. Pamiętaj, że w spektroskopii nie mamy do czynienia z jedną cząsteczką. Mamy do czynienia z ogromną liczbą cząsteczek. Niektóre cząsteczki będą w jednej sytuacji. Niektóre cząsteczki będą w innej sytuacji. Zobaczymy obie sytuacje. Będzie absorbancja przy dwóch różnych natężeniach pola magnetycznego.

w rezultacie widmo EPR pokazuje dwa piki, w ten sposób:
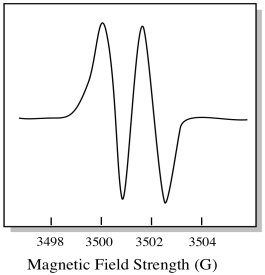
ten typ piku w widmie nazywa się dubletem, ze względu na podwójną absorbancję. Ta cecha piku EPR nazywana jest jego wielokrotnością. Na ile linii jest podzielony szczyt? Dwa. To dublet.
wszystko jest jeszcze ciekawsze, jeśli w pobliżu znajdują się dwa protony. W takim przypadku oba sąsiednie protony mają spin. Każdy obrót może mieć wartość +1/2 lub -1/2. Może oba są +1/2. Może oba są -1 / 2. Może jest po jednym z każdego. Te trzy możliwe kombinacje będą miały trzy różne skutki dla pola magnetycznego doświadczanego przez elektron.
w rezultacie w widmie występują trzy piki. Widmo nazywa się triplet. Ten tryplet jest pokazany poniżej, pod diagramem, który ilustruje kombinacje spinów sąsiednich wodorów.
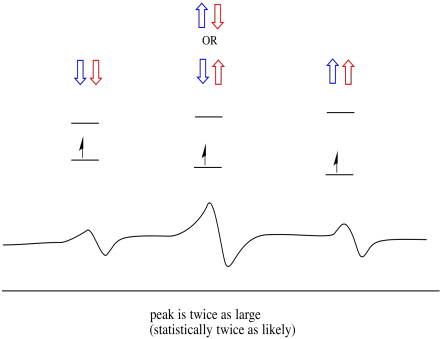
zauważ, że ponieważ wodór może być w górę lub w dół w mieszanej kombinacji, istnieją dwa sposoby osiągnięcia tego stanu środkowego. Ta kombinacja jest dwa razy bardziej prawdopodobna niż pozostałe dwa, ponieważ jest tylko jeden sposób uzyskania tej kombinacji: obroty obu atomów wodoru są większe, w jednym przypadku. Oba hydrogeny są w drugim. W rezultacie środkowy szczyt w trójlistku jest dwa razy większy od szczytów na krawędziach.
ćwiczenie \(\PageIndex{1}\)
pokazuje, że z trzema sąsiadującymi wodorami powstaje kwartet, w którym proporcje pików wynoszą 1:3:3:1.
odpowiedź
kombinacje są:
a) wszystkie obroty są w dół (i jest tylko jeden sposób, aby to zrobić)
b) dwa obroty są w dół, ale jeden jest w górę (i każdy z trzech protonów może być w górę, więc są trzy sposoby)
c) dwa obroty są w górę, ale jeden jest w dół (i każdy z trzech protonów może być w dół, więc są trzy sposoby)
d) wszystkie obroty są w górę (i jest tylko jeden sposób, aby to zrobić)
to).
wynikiem 1:3:3:1.
ćwiczenie \(\PageIndex{2}\)
przewiduj wielokrotność w widmie EPR dla każdego z następujących rodników alkoksylowych (zauważ, że tlen i węgiel nie mają niesparowanych spinów; Załóżmy, że to samo dotyczy x):
A) X3C-o. b) X2CH-O. c) XCH2-O. d) CH3-O.
odpowiedź a)
a) singlet
odpowiedź b)
b) dublet
odpowiedź C)
C) triplet
odpowiedź D)
D) kwartet
ćwiczenie \(\pageindex{3}\)
przypuśćmy, że benzen został zredukowany o jeden elektron, aby otrzymać anion rodnikowy benzenu. Jaka byłaby wielość widma EPR?
Odpowiedz
A septet (w 1:3:5:7:5:3:1 stosunek).
sprzężenie z jonami metali
wiele jąder innych niż wodór ma spin sieciowy. Jeśli niesparowany elektron zostanie znaleziony na metalu, widmo EPR może dostarczyć potwierdzenia tej informacji strukturalnej. Potwierdzenie To może pochodzić zarówno z informacji o polu magnetycznym (podobnie jak przesunięcie chemiczne w NMR), jak i z wielokrotności.
spiny jądrowe wybranych metali przedstawiono poniżej.
| Metal | Spin |
| V | 7/2 |
| Mn | 5/2 |
| Fe | 0 |
| co | 7/2 |
| cu | 3/2 |
w każdym z tych metali jądro ma różne możliwe pola magnetyczne. Zauważ, że ich działanie jest nieco bardziej skomplikowane niż działanie atomu wodoru. Na przykład miedź o spinie 3/2 działa trochę jak trzy różne jądra wodoru (każde o spinie + / – 1/2) pod względem swojego wpływu na widmo EPR pobliskiego elektro. Wielokrotność niesparowanego elektronu na Jonie miedzi powinna być dość charakterystyczna.
ćwiczenie \(\PageIndex{4}\)
Przewidywanie wielokrotności piku w widmie EPR dla niesparowanego elektronu na każdym z następujących metali:
a) wanad b) mangan c) żelazo d) kobalt e) miedź
odpowiedź A)
A) oktet (w 1:3:5:7:7:5:3:1 stosunek)
odpowiedź B)
B) sekstet (w 1:3:5:5:3:1 ratio)
odpowiedź C)
C) singlet
odpowiedź D)
D) oktet
Odpowiedź e)
e) kwartet (w stosunku 1:3:3:1)
czasami rzeczy są bardziej skomplikowane, ponieważ różne izotopy tego samego pierwiastka mogą mieć różne możliwe wartości spinu. W rzeczywistości jest to prawdą w przypadku wodoru i węgla, ale zdecydowana większość wodoru znajduje się w 1H, więc ogólnie możemy myśleć o tym, że ma spin = 1/2; zdecydowana większość węgla to 12C, ze spinem = 0.
naturalne izotopy żelaza i ich spiny jądrowe przedstawiono w poniższej tabeli.
| Isotope | Spin | % Abundance |
| 54Fe | 0 | 5.9 |
| 56Fe | 0 | 91.8 |
| 57Fe | 1/2 | 2.1 |
| 58Fe | 0 | 0.2 |
The EPR spectrum of an unpaired electron on iron may be slightly more complicated than we first thought. W próbce część elektronów byłaby położona na jonach żelaza o spinie = 1/2, chociaż większość nie. Ta komplikacja może być wystarczająca, aby wprowadzić niewielką zmianę w wyglądzie widma,ale ogólnie nadal wyglądałaby prawie jak singiel.
jednak w wielu przypadkach sprawy stają się znacznie bardziej złożone. Molibden stanowi dobry przykład.
| izotop | Spin | % obfitości |
| 92Mo | 0 | 14.8 |
| 94mo | 0 | 9.3 |
| 95Mo | 5/2 | 15, 9 |
| 96Mo | 0 | 16, 7 |
| 97Mo | 5/2 | 9, 6 |
| 98mo | 0 | 24, 1 |
| 100Mo | 0 |
istnieje siedem naturalnie występujących izotopów molibdenu. Pięć z nich ma spin = 0, więc niesparowany elektron na tych izotopach dałby początek prostemu singletowi w widmie EPR. Pozostałe dwa izotopy, stanowiące 25% całości, mają spin = 5/2. Większość niesparowanych elektronów na molibdenu pojawi się jako singlet. Jednak znaczna część pojawiłaby się jako sekstet. Oznacza to, że w idealnym przypadku niesparowany elektron na molibdenu spowodowałby powstanie singletu z nałożonym na niego sekstetem (około jednej czwartej tak silnym jak singlet).
ta sytuacja może wyglądać mniej więcej tak jak na rysunku poniżej.
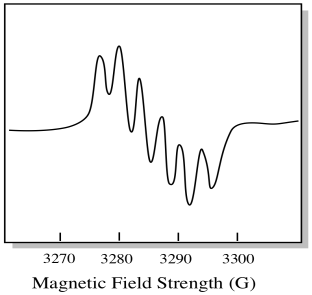
w rzeczywistości widma EPR są w wielu przypadkach ogromnie skomplikowane. Często wyglądają jak rozmyte plamy. Istnieje tak wiele rzeczy, które łączą się z tak wieloma innymi rzeczami, że staje się prawie niemożliwe do rozszyfrowania na oko. W większości przypadków symulacje komputerowe są uruchamiane, a dane eksperymentalne są porównywane z symulacjami komputerowymi w celu uzyskania wglądu strukturalnego.
ćwiczenie \(\PageIndex{5}\)
wanad jest obecny w niektórych nitrogenazach i dlatego zainteresowanie modelowymi kompleksami (np. Sandro Gambarotta i wsp., J. am. Chem. Soc. 1994, 116, 6927-6928). Gambarotta zastosował następującą syntezę, w rozpuszczalniku THF:
\(\ce{vcl3 + k- >3V (THF)}\)
- narysuj strukturę produktu reakcji.
- narysuj diagram dzielenia orbitali D dla tego kompleksu.
- dla tego związku zarejestrowano widmo EPR. Naszkicuj widmo, biorąc pod uwagę, że wanad ma spin jądrowy I = 7/2.
- oszacuj µeff dla tego związku.
związek reaguje z N2, tworząc dimer mostkowany N2.
e) narysuj strukturę tego produktu.
f) związek ten nie wytwarza widma EPR. Podaj strukturę rezonansową (e), która wyjaśnia tę obserwację.
odpowiedź
widma EPR udostępnione dzięki uprzejmości Virtual Imagination / Slapdash Chemistry Creations.
Atrybucja
Chris P Schaller, Ph. D., (College of Saint Benedict / Saint John ’ s University)