Forme posologique: Injection
Revue médicale par Drugs.com . Dernière mise à jour le 22 mai 2020.
- Overview
- Side Effects
- Dosage
- Professional
- Interactions
- More
FOR USE IN NERVE AGENT POISONING ONLY
A Sterile Solution For Intramuscular Use Only
Rx Only
- Pralidoxime Chloride Description
- Chlorure de Pralidoxime – Pharmacologie clinique
- Indications et utilisation pour le Chlorure de Pralidoxime
- Contre-indications
- Avertissements
- Précautions
- Généralités:
- Information pour les patients:
- Tests de laboratoire:
- Interactions médicamenteuses:
- Carcinogenèse, Mutagensis, Altération de la fertilité:
- Grossesse
- Mère allaitante:
- Utilisation pédiatrique:
- Effets indésirables
- Toxicomanie et dépendance
- Surdosage
- Manifestations de surdosage:
- Traitement du surdosage:
- Acute Toxicity:
- Posologie et administration du chlorure de Pralidoxime
- Mode d’emploi:
- Comment est fourni le chlorure de Pralidoxime
- Panneau d’affichage principal – Injection de chlorure de Pralidoxime, Étiquette de 300 mg
- En savoir plus sur la pralidoxime
- Ressources pour les consommateurs
- Ressources professionnelles
- Guides de traitement connexes
Pralidoxime Chloride Description
Pralidoxime Chloride Injection (auto-injector) provides Pralidoxime Chloride in a sterile solution for intramuscular injection.
Chaque auto-injecteur prérempli fournit une dose de l’antidote, le chlorure de Pralidoxime dans une unité autonome, spécialement conçue pour l’auto-administration automatique ou l’administration en binôme par le personnel militaire. La pralidoxime dans l’auto-injecteur peut également être administrée par des intervenants civils qualifiés qui ont reçu une formation adéquate sur la reconnaissance et le traitement sur place de l’intoxication par un agent neurotoxique en cas de libération accidentelle d’un agent neurotoxique. La procédure recommandée (voir POSOLOGIE ET ADMINISTRATION) consiste à injecter le contenu de l’auto-injecteur dans les muscles d’une cuisse externe.
Une fois qu’un auto-injecteur a été activé, le récipient vide doit être éliminé correctement (voir POSOLOGIE ET ADMINISTRATION), il ne peut pas être rempli ni l’aiguille en saillie ne peut être rétractée.
Lorsqu’il est activé, chaque auto-injecteur distribue 600 mg de chlorure de Pralidoxime dans 2 mL d’une solution stérile contenant 20 mg / mL d’alcool benzylique, 11,26 mg / mL de glycine dans de l’eau pour injection, USP. Le pH est ajusté avec de l’acide chlorhydrique. La plage de pH est de 2,0 à 3,0. Le produit est sans pyrogène.
Le chlorure de pralidoxime est un réactivateur de la cholinestérase.
Nom chimique: oxime de chlorure de 2-formyl-1 méthylpyridinium (méthochlorure de pyridine-2 aldoxime). Également appelé chlorure de 2-PAM.
Formule structurelle:
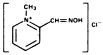
Le chlorure de pralidoxime se présente sous la forme d’une poudre cristalline inodore, blanche, non hygroscopique, soluble dans l’eau à raison de 1 g dans moins de 1 mL. Stable à l’air, il fond entre 215°C et 225°C, avec décomposition.
L’activité spécifique du médicament réside dans l’ion 2-formyl-1 méthylpyridinium et est indépendante du sel particulier utilisé. Le chlorure est préféré en raison de sa compatibilité physiologique, de son excellente solubilité dans l’eau à toutes les températures et de sa puissance élevée par gramme, en raison de son faible poids moléculaire (173).
Chlorure de Pralidoxime – Pharmacologie clinique
Le chlorure de Pralidoxime est un réactivateur de la cholinestérase.
L’action principale de la pralidoxime est de réactiver la cholinestérase (principalement en dehors du système nerveux central) qui a été inactivée par phosphorylation due à un pesticide organophosphoré ou à un composé apparenté. La destruction de l’acétylcholine accumulée peut alors se poursuivre et les jonctions neuromusculaires fonctionneront à nouveau normalement. La pralidoxime ralentit également le processus de « vieillissement » de la cholinestérase phosphorylée en une forme non réactivable et détoxifie certains organophosphorés par réaction chimique directe. Le médicament a son effet le plus critique pour soulager la paralysie des muscles de la respiration. Parce que la pralidoxime est moins efficace pour soulager la dépression du centre respiratoire, l’atropine est toujours nécessaire de manière concomitante pour bloquer l’effet de l’acétylcholine accumulée à ce site. La pralidoxime soulage les signes et symptômes muscariniques, la salivation, le bronchospasme, etc., mais cette action est relativement peu importante car l’atropine est adéquate à cet effet.
La pralidoxime est distribuée dans toute l’eau extracellulaire, elle n’est pas liée aux protéines plasmatiques. Le médicament est rapidement excrété dans l’urine en partie sous forme inchangée et en partie sous forme de métabolite produit par le foie. Par conséquent, la pralidoxime a une action relativement courte et des doses répétées peuvent être nécessaires, en particulier lorsqu’il existe des preuves d’absorption continue du poison.
La concentration thérapeutique minimale de pralidoxime dans le plasma est de 4 µg / mL, ce niveau est atteint en environ 16 minutes après une seule injection de 600 mg de chlorure de Pralidoxime. La demi-vie apparente du chlorure de Pralidoxime est de 74 à 77 minutes.
Il a été rapporté que l’utilisation supplémentaire de réactivateurs de la cholinestérase de l’oxime (tels que la pralidoxime) réduit l’incidence et la gravité des anomalies du développement chez les embryons de poussin exposés à des tératogènes connus tels que le parathion, la bidrine, le carbachol et la néostigmine. Il a été démontré que cet effet protecteur des oximes était lié à la dose.
Indications et utilisation pour le Chlorure de Pralidoxime
Cet auto-injecteur pour le chlorure de Pralidoxime est spécifiquement indiqué pour une utilisation intramusculaire en complément de l’atropine dans le traitement de l’empoisonnement par des agents neurotoxiques ayant une activité anticholinestérasique.
Contre-indications
L’auto-injecteur de chlorure de Pralidoxime est contre-indiqué chez les patients présentant une hypersensibilité à l’un des composants du produit.
Avertissements
La pralidoxime n’est pas efficace dans le traitement des intoxications dues au phosphore, aux phosphates inorganiques ou aux organophosphates n’ayant pas d’activité anticholinestérasique.
Précautions
Généralités:
La pralidoxime a été très bien tolérée dans la plupart des cas, mais il ne faut pas oublier que l’état désespéré du patient empoisonné aux organophosphorés masquera généralement les signes et symptômes mineurs observés chez les sujets normaux.
Comme la pralidoxime est excrétée dans l’urine, une diminution de la fonction rénale entraînera une augmentation des taux sanguins du médicament. Ainsi, la posologie de pralidoxime doit être réduite en présence d’insuffisance rénale.
Information pour les patients:
L’auto-injecteur de chlorure de Pralidoxime doit être auto-administré par du personnel militaire ou administré par des intervenants d’urgence civils qualifiés uniquement après que les événements suivants se sont produits:
– l’individu a enfilé son masque après avoir reconnu l’existence d’un danger d’agent chimique dans sa région – certains ou la totalité des symptômes d’empoisonnement aux agents neurotoxiques cités ci-dessous sont présents: nez qui coule inexpliqué oppression thoracique avec difficulté à respirer pupilles repérées de l’œil entraînant une vision floue bave, une transpiration excessive nausées, vomissements et crampes abdominales mictions et défécations involontaires secousses, contractions et vertiges maux de tête, somnolence, coma, convulsions Arrêt de la respiration
Des mesures appropriées doivent être prises pour que le personnel équipé d’auto-injecteurs comprenne leurs indications et leur utilisation, y compris l’examen des symptômes d’empoisonnement et le fonctionnement de l’auto-injecteur.
Tests de laboratoire:
Le traitement de l’empoisonnement aux organophosphorés doit être instauré sans attendre les résultats des tests de laboratoire. Les mesures des globules rouges, de la cholinestérase plasmatique et du paranitrophénol urinaire (en cas d’exposition au parathion) peuvent être utiles pour confirmer le diagnostic et suivre l’évolution de la maladie. Une réduction de la concentration de cholinestérase des globules rouges à moins de 50% de la normale n’a été observée qu’avec un empoisonnement à l’ester organophosphoré.
Interactions médicamenteuses:
Lorsque l’atropine et la pralidoxime sont utilisées ensemble, les signes d’atropinisation (bouffées vasomotrices, mydriase, tachycardie, sécheresse de la bouche et du nez) peuvent survenir plus tôt que prévu lorsque l’atropine est utilisée seule. Cela est particulièrement vrai si la dose totale d’atropine a été importante et que l’administration de pralidoxime a été retardée.2, 3, 4
Les précautions suivantes doivent être prises dans le traitement de l’intoxication par l’anticholestérinase, bien qu’elles ne portent pas directement sur l’utilisation du pralidoxime; étant donné que les barbituriques sont potentialisés par les anticholinestérases, ils doivent être utilisés avec prudence dans le traitement des convulsions; les tranquillisants de type morphine, théophylline, aminophylline, succinylcholine, reser-pin et phénothiazine doivent être évités chez les patients intoxiqués par des organophosphorés.
Carcinogenèse, Mutagensis, Altération de la fertilité:
Étant donné que l’auto-injecteur de chlorure de Pralidoxime est indiqué pour une utilisation d’urgence à court terme seulement, aucune étude de son potentiel de carcinogenèse, de mutagenèse ou d’altération de la fertilité n’a été menée par le fabricant ou rapportée dans la littérature.
Grossesse
Aucune étude de reproduction chez l’animal n’a été menée avec la pralidoxime. On ne sait pas non plus si la pralidoxime peut causer des dommages fœtaux lorsqu’elle est administrée à une femme enceinte ou peut affecter la capacité de reproduction. Pralidoxime ne doit être administré à une femme enceinte que si cela est clairement nécessaire.
Mère allaitante:
On ne sait pas si ce médicament est excrété dans le lait maternel. Étant donné que de nombreux médicaments sont excrétés dans le lait maternel, des précautions doivent être prises lorsque la pralidoxime est administrée à une femme qui allaite.
Utilisation pédiatrique:
L’innocuité et l’efficacité chez les enfants n’ont pas été établies.
Effets indésirables
Quarante à 60 minutes après l’injection intramusculaire, une douleur légère à modérée peut être ressentie au site d’injection.
La pralidoxime peut provoquer une vision trouble, une diplopie et une altération de l’accommodation, des étourdissements, des maux de tête, une somnolence, des nausées, une tachycardie, une augmentation de la pression artérielle systolique et diastolique, une hyperventilation et une faiblesse musculaire lorsqu’elle est administrée par voie parentérale à des volontaires normaux qui n’ont pas été exposés à des poisons anticholinestérasiques. Chez les patients, il est très difficile de différencier les effets toxiques produits par l’atropine ou les composés organophosphorés de ceux du médicament.
Des élévations des taux d’enzymes SGOT et/ou SGPT ont été observées chez 1 des 6 volontaires normaux recevant 1200 mg de chlorure de Pralidoxime par voie intramusculaire et chez 4 des 6 volontaires recevant 1800 mg par voie intramusculaire. Les niveaux sont revenus à la normale en environ 2 semaines. Des élévations transitoires de la créatine phosphokinase ont été observées chez tous les volontaires normaux ayant reçu le médicament. Une seule injection intramusculaire de 330 mg dans 1 mL chez le lapin a provoqué une myonécrose, une inflammation et une hémorragie.
Lorsque l’atropine et la pralidoxime sont utilisées ensemble, les signes d’atropinisation peuvent survenir plus tôt que prévu lorsque l’atropine est utilisée seule. Cela est particulièrement vrai si la dose totale d’atropine a été importante et que l’administration de pralidoxime a été retardée.2, 3, 4 L’excitation et le comportement maniaque immédiatement après la récupération de la conscience ont été rapportés dans plusieurs cas. Cependant, un comportement similaire s’est produit dans les cas d’empoisonnement aux organophosphorés qui n’ont pas été traités par la pralidoxime.3, 5, 6
Toxicomanie et dépendance
Le chlorure de pralidoxime n’est pas sujet à abus et ne présente aucun potentiel connu de dépendance.
Surdosage
Manifestations de surdosage:
Observées chez des sujets normaux uniquement: vertiges, vision floue, diplopie, maux de tête, troubles de l’accommodation, nausées, légère tachycardie. En thérapie, il a été difficile de différencier les effets secondaires dus au médicament de ceux dus aux effets du poison.
Traitement du surdosage:
La respiration artificielle et d’autres traitements de soutien doivent être administrés au besoin.
Acute Toxicity:
i.v.—man TDLo: 14 mg/kg (toxic effects: CNS) i.v.— rat LD50: 96 mg/kg i.m.—rat LD50: 150 mg/kg oral—mouse LD50: 4100 mg/kg i.p.—mouse LD50: 155 mg/kg i.v.—mouse LD50: 90 mg/kg i.m.—mouse LD50: 180 mg/kg i.v.—rabbit LD50: 95 mg/kg i.m.—guinea pig LD50: 168 mg / kg
Posologie et administration du chlorure de Pralidoxime
Exposition à des agents neurotoxiques possédant une activité anticholinestérasique (type organophosphate)
LÉGÈRE céphalée de CAS, vision floue, signes muscariniques légers
MODÉRÉMENT SÉVÈRE CAS — transpiration excessive, larmoiement, salivation, diarrhée, oppression thoracique
Pour une réactivation optimale de la cholinestérase inhibée par les organophosphates, de l’atropine et de la le pralidoxime doit être administré dès que possible après l’exposition. Selon la gravité des symptômes, administrer immédiatement un auto-injecteur contenant de l’atropine, suivi d’un auto-injecteur contenant du pralidoxime. L’atropine doit d’abord être administrée jusqu’à ce que ses effets deviennent apparents et ce n’est qu’alors que le pralidoxime doit être administré. Si les symptômes de l’agent neurotoxique sont toujours présents après 15 minutes, répétez les injections. Si les symptômes persistent après 15 minutes supplémentaires, répétez les injections une troisième fois. Si après la troisième série d’injections, les symptômes persistent, ne donnez plus d’antidotes mais consultez un médecin.
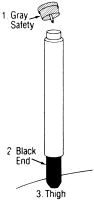
Mode d’emploi:
Lorsque, comme décrit ci-dessus, l’utilisation de l’auto-injecteur est indiquée, procédez comme suit:
|
 |
CAS TRÈS GRAVE — Cyanose, maladie respiratoire Gêne, Coma
Les mesures initiales devraient inclure l’élimination des sécrétions, le maintien d’une voie aérienne brevetée et, si nécessaire, une ventilation artificielle. L’atropine ne doit pas être utilisée tant que la cyanose n’a pas été surmontée, car l’atropine produit des fibrillations ventriculaires en présence d’hypoxie. La morphine, la théophylline, l’aminophylline ou la succincylcholine sont contre-indiquées. Les tranquillisants de type réserpine ou phénothiazine sont à éviter.
« Le pralidoxime est le plus efficace s’il est administré immédiatement après l’empoisonnement. Généralement, peu de choses sont accomplies si le médicament est administré plus de 36 heures après la fin de l’exposition. Cependant, lorsque le poison a été ingéré, l’exposition peut se poursuivre pendant un certain temps en raison d’une absorption lente de l’intestin inférieur, et des rechutes fatales ont été rapportées après une amélioration initiale. Une administration continue pendant plusieurs jours peut être utile chez ces patients. Une surveillance étroite du patient est indiquée pendant au moins 48 à 72 heures. En cas d’exposition cutanée, les vêtements doivent être enlevés et les cheveux et la peau soigneusement lavés avec du bicarbonate de sodium ou de l’alcool dès que possible. Le diazépam peut être administré avec prudence si les convulsions ne sont pas contrôlées par l’atropine. »7
IMPORTANT : LES MÉDECINS ET/OU TOUT AUTRE PERSONNEL MÉDICAL AIDANT LES VICTIMES ÉVACUÉES D’AGENTS NEUROTOXIQUES DEVRAIENT ÉVITER DE S’EXPOSER À LA CONTAMINATION PAR LES VÊTEMENTS DES VICTIMES.
Comment est fourni le chlorure de Pralidoxime
Le chlorure de Pralidoxime est fourni en solution aqueuse préremplie dans l’auto-injecteur (600 mg, 2 mL) pour un usage militaire et pour une utilisation par des intervenants d’urgence civils qualifiés. Les auto-injecteurs sont fournis par la Direction du Matériel médical, le Centre d’approvisionnement de la Défense de Philadelphie ou toute autre agence locale, étatique ou fédérale analogue.
Lorsqu’il est activé, chaque auto-injecteur distribue 600 mg de chlorure de Pralidoxime dans 2 mL d’une solution stérile contenant 20 mg / mL d’alcool benzylique, 11,26 mg / mL de glycine dans de l’eau pour injection, USP. Le pH est ajusté avec de l’acide chlorhydrique. Le pH est de 2,0-3,0 Le produit est sans pyrogène.
Conserver à 25 °C (77 °F); Excursions autorisées à 15-30 °C (59-86 °F).
Ne pas geler.
Meridian Medical Technologies, Inc.
Columbia, MD 21046
A Pfizer Company
00001976
08/16
Imprimé aux États-Unis
- Landauer, W.: Tétrogènes cholinomimétiques. V. The effect of oximes and related cholinesterase reactivators, Tératologie 15:33 (Fév.) 1977.
- Moller, K. O., Jenson-Holm, J., et Lausen, H. H.: Ugeskr. Laeg.123:501, 1961.
- Namba, T., Nolte, C.T., Jackrel, Jr., et Grob, D.: Empoisonnement dû aux insecticides organophosphorés. Manifestations aiguës et chroniques, Amer. J. Med. 50:475 (Avr.) 1971.
- Arena, J. M.: Empoisonnement. Toxicologie. Symptômes. Traitements, ed. 4, Springfield, Illinois., Charles C. Thomas, 1979, p. 133.
- Brachfeld, J., et Zavon, M. R. : Intoxication au phosphate organique (Phosdrine®). Rapport de cas et résultats du traitement par 2-PAM, Arch. Environ. Santé 11: 859,1965.
- Hayes, W. J., Jr. : Toxicologie des pesticides, Baltimore, The Williams&Wilkins Company, 1975, p. 416.
- Département des médicaments de l’AMA: Évaluations des médicaments de l’AMA, éd. 4, Chicago, Association médicale américaine, 1980, p. 1455.
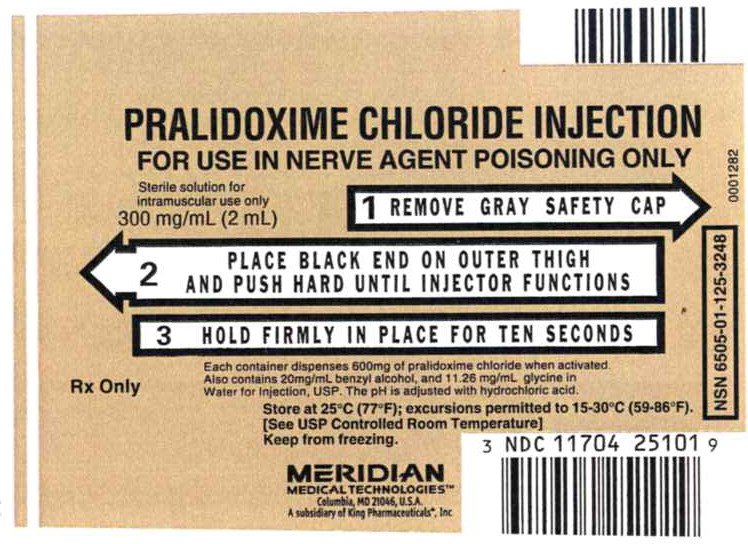
Panneau d’affichage principal – Injection de chlorure de Pralidoxime, Étiquette de 300 mg
NDC 11704-107-01
INJECTION DE chlorure de Pralidoxime
À UTILISER UNIQUEMENT EN CAS D’INTOXICATION PAR UN AGENT NEUROTOXIQUE
Solution stérile pour usage intramusculaire seulement
300 mg/mL (2 mL)
1 RETIRER LE CAPUCHON DE SÉCURITÉ GRIS
2 PLACEZ L’EXTRÉMITÉ NOIRE SUR LA CUISSE EXTÉRIEURE ET POUSSEZ FORT JUSQU’À CE QUE L’INJECTEUR FONCTIONNE
3 MAINTENEZ FERMEMENT EN PLACE PENDANT DIX SECONDES
Chaque contenant distribue 600 mg de chlorure de Pralidoxime lorsqu’il est activé.
Contient également 20 mg/mL d’alcool benzylique et 11.26 mg/mL de glycine dans
Eau pour injection, USP. Le pH est ajusté avec de l’acide chlorhydrique.
Rx Uniquement
Conserver à 25 °C (77 °F); excursions autorisées à 15-30 °C (59-86 °F).
Ne pas congeler.
MERIDIAN MEDICAL TECHNOLIGIESTM
Columbia, MD 21046, USA
A subsidiary of King Pharmaceuticals®, Inc
NDC 11704-251-01
NSN 6505-01-125-3248
| Pralidoxime Chloride Pralidoxime Chloride injection |
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
Labeler – Meridian Medical Technologies, Inc. (167671341)
| Establishment | |||
| Name | Address | ID/FEI | Operations |
| Meridian Medical Technologies, Inc. | 038889234 | MANUFACTURE(11704-251), ANALYSIS(11704-251) | |
| Establishment | |||
| Name | Address | ID/FEI | Operations |
| Meridian Medical Technologies, Inc. | 078808315 | MANUFACTURE(11704-251), LABEL(11704-251), PACK(11704-251) | |
| Establishment | |||
| Name | Address | ID/FEI | Operations |
| Meridian Medical Technologies, Inc. | 167671341 | MANUFACTURE(11704-251), LABEL(11704-251), PACK(11704-251), ANALYSIS(11704-251) | |
En savoir plus sur la pralidoxime
- Effets secondaires
- Pendant la grossesse
- Informations posologiques
- Interactions médicamenteuses
- En Español
- Classe de médicament: antidotes
- Alertes de la FDA (1)
Ressources pour les consommateurs
- Informations sur le patient
- Injection de Pralidoxime (Lecture avancée)
Ressources professionnelles
- Informations sur la prescription
- Pralidoxime (Conseils professionnels aux patients)
Autres marques Protopam Chloride
Guides de traitement connexes
- Surdosage en anticholinestérase
- Empoisonnement aux organophosphorés
- Empoisonnement aux agents neurotoxiques
Avertissement médical