Hvis du udvikler produkter — især medicinsk udstyr — så har du hørt udtrykkene designvalidering og designverifikation (også kaldet V& V). Her forklarer vi, hvad de to aktiviteter er, forskellen mellem dem, plus del tip til at få mest muligt ud af din indsats.
Bemærk: For at validere, at dette indhold ville være nyttigt for dig, har vi forbindelse til Megan Martin, en medicinsk enhed V&V konsulent med over 30 års erfaring inden for medicinsk udstyr V&V, medicinsk udstyrsprogram, produkt-og programmelkvalitet og amerikanske og internationale enhedsregulerende indlæg. Du finder hendes indsigt og eksempler overalt!
Følg med eller spring til det afsnit, du leder efter:
- Designvalidering vs. Designverifikation
- hvad er Designvalidering nøjagtigt?
- hvad er Design verifikation for FDA?
- Validering vs Verifikationsoversigt
- Grundlæggende om Designvalideringsproces
- Grundlæggende om Designverifikationsproces
- 6 tip til bedre Validering & verifikation
- Video: forenkle V & V
- V&V: ordliste
- designvalidering vs. designverifikation: hvad er forskellen?
- Hvad er Designvalidering nøjagtigt?
- eksempel på Designvalidering
- brugerbehov
- hvad er Design verifikation for FDA?
- eksempel på Designbekræftelse
- produktkrav
- designspecifikationer
- Validering vs Verifikationsoversigt
- Grundlæggende om Designvalideringsproces
- Grundlæggende om Designverifikationsproces
- identificering og forberedelse
- planlægning
- udvikling
- udførelse af
- rapportering
- 6 tip til bedre Validering & verifikation
- Planlæg fremad (og Test tidligt)
- brug delt nomenklatur
- brug værktøjer med End-to-End sporbarhed
- Byg din Sporingsmatrice, mens du går
- Integrer krav sporbarhed& test med anomali Tracking
- Vælg Værktøjer, du kan tilpasse til din metode
- at bringe det hele sammen
- forenkle V&V med spiral ALM
- V& V: ordliste
- fælles Designvalidering akronymer
designvalidering vs. designverifikation: hvad er forskellen?
Hvad er forskellen mellem validering og verifikation? Kort sagt, designvalidering bestemmer, om du bygger det rigtige produkt. Fungerer enheden som beregnet til slutbrugerne? Designbekræftelse bestemmer, om du bygger produktet rigtigt. Matcher designudgange designindgange?
det er den enkle forskel som tydeligt afbildet i grafen nedenfor.
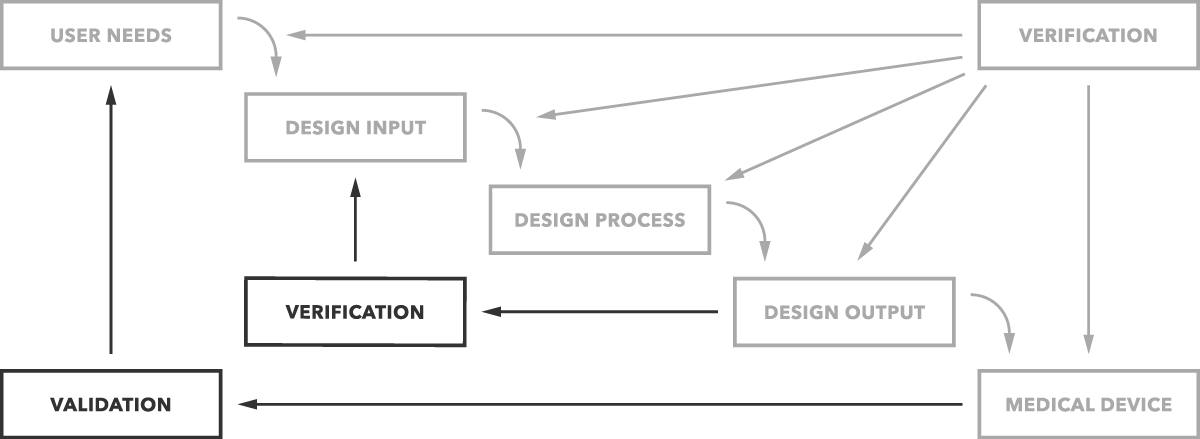
men du vil selvfølgelig have flere detaljer og eksempler. Vi begynder med validering.
Hvad er Designvalidering nøjagtigt?
designvalidering er en testproces, hvor du beviser (“validerer”), at den enhed, du har bygget, fungerer for slutbrugeren som beregnet.
officielt ord fra FDA (21 CFR 820.3) siger, at designvalidering er “ved objektiv bevis for, at enhedsspecifikationer er i overensstemmelse med brugernes behov og tilsigtede anvendelse(er).”
eksempel på Designvalidering
lad os forestille os, at vi bygger en ventilator, der holder en patient vejrtrækning, og at brugeren ønsker, at den skal fungere under patienttransport.
først skal vi definere vores brugerbehov. Brugeren ønsker at flytte patienter, mens de er på ventilatoren. Men hvad prøver de faktisk at gøre? “Transport” kan omfatte flytning af patienten på hospitalet. Eller kan omfatte transport via ambulance eller med fly. Et brugerbehov kan for eksempel se ud som følgende.
brugerbehov
| UsNe-0001 | ventilatoren er egnet til brug under hospitalstransport af patienter. |
dette brugerbehov vil blive opdelt i produktkrav og designspecifikationer for at designe og bygge produktet. (Vi vil se på dem i et øjeblik under design verifikation.)
før det, lad os undersøge vores brugerbehov og se, hvilke designvalideringstestsager der kan være påkrævet. Valideringstest af vores brugerbehov kan se sådan ud.
| bruger behov |
Validering Test |
||
|---|---|---|---|
| usne-0001 | ventilatoren er egnet til brug under hospitalstransport af patienter. | TCase-0001 | valideringstest Suite: Test, at ventilatoren let kan rulles af 15 medlemmer af hospitalets transportpersonale. |
| TCase-0002 | Validering Test Suite: Test, at ventilatoren fungerer inden for dens specifikationer, mens den rulles ned ad gange, over dørstop, og over elevatortærskler. | ||
| TCase-0003 | Validering Test Suite: Test, at ventilatoren fungerer inden for dens specifikationer, mens overgangen mellem vekselstrøm og batteridrift. | ||
valideringstest vil omfatte testcases, test suiter eller endda kliniske forsøg designet til at bevise, at produktet, som bygget, fungerer i overensstemmelse med brugerens forventninger under de betingelser, hvor de agter at bruge det. Da disse test skal køres på produktions-eller produktionsækvivalente enheder, er designvalideringstest ofte de sidste test, der udføres.
grundlæggende skal vi i designvalidering demonstrere, at produktet opfylder brugerens behov.
forresten viser tabellen ovenfor også sporbarheden mellem brugerbehov og testsager. Denne spormatrice giver en del af V&V bevis for, at FDA kræver.
hvad er Design verifikation for FDA?
Designverifikation er det sted, hvor du tester (“bekræft”), at dine designudgange matcher dine designindgange.
igen er designverifikation ifølge FDA “bekræftelse ved undersøgelse og tilvejebringelse af objektiv dokumentation for, at specificerede krav er opfyldt.”
Husk, at selvom det vil involvere test, er der andre acceptable verifikationsaktiviteter.
de kan omfatte test, inspektioner og analyser (for mere om dette, tjek FDA Design Control Guidance).
eksempel på Designbekræftelse
lad os vende tilbage til vores ventilatoreksempel. Vi har identificeret vores brugerbehov; lad os nu identificere, hvad enheden skal gøre, og hvordan den skal gøre det.
for at opnå det skal vi definere specifikke produktkrav. For eksempel:
- hvad er maksimal belastning for en patient? (Hvor meget luft skal ventilatoren flytte?)
- hvor længe skal batteriet vare? (Hvor lang tid tager transport?)
- hvilke forhold vil de støde på under transport? (Dør syltetøj? Elevatorer?)
- er der nogen lovgivningsmæssige standarder, der skal opfyldes? (Sikkerhedsstandarder?)
“klare, komplette, entydige, testbare krav er en nøglekomponent i et vellykket udviklingsprojekt. Utilstrækkelige krav fører til spildt tid, designfejl, omfattende omarbejdning og skrøbelige eller fejlbehæftede produkter.”- Megan Martin, v &V konsulent
Dette er “hvad” del af at definere enhedens egenskaber. Hvad skal enheden nøjagtigt gøre? Produktkrav (ofte inkluderet i et produktkravsdokument) til vores brugerbehov kan se ud som nedenfor.
produktkrav
|
Prrk-0001 |
ventilatoren skal have en maksimal indstilling af 2-liters volumenstyrede vejrtrækninger ved 20 vejrtrækninger pr.minut. |
|
PRR-0002 |
ventilatoren skal køre på batteristrøm ved maksimale indstillinger i mindst 90 minutter. |
|
PRR-0003 |
ventilatoren skal kunne monteres på et rullestativ. |
|
PRR-0004 |
ventilatoren og stativet skal kunne krydse typiske tærskler for hospitalsdøre og elevatorer. |
endelig har vi brug for designspecifikation. “Vi har allerede defineret, hvad vi skal opnå, og nu skal vi definere, hvordan vi skal gøre det,” siger Megan. Dette kan opnås på forskellige måder, herunder skriftlige specifikationer, elektriske eller mekaniske tegninger, komponentkøbsspecifikationer eller andre metoder.
for eksempel kan designspecifikationerne og tegningerne vise følgende.
designspecifikationer
|
DSpec-0001 |
en turbine, der kan generere op til 40 liter luft pr. |
|
DSpec-0002 |
en lithium-ion-batteripakke, der er klassificeret i mindst 100 Amp-Timer. |
|
DSpec-0003 |
monteringen til rullestativet bruger en stålhåndtagsklemme, der er klassificeret til 22 lbs. |
|
DSpec-0004 |
stativbasen er 22″ bred med 5 hjul. |
|
DSpec-0005 |
stativhjulene har en diameter på 4″. |
designverifikation giver bevis (testresultater) for, at designudgangene (faktisk produkt) opfylder designindgangene (produktkrav og designspecifikationer). Afhængigt af det element, der verificeres, vil en testsag eller testpakke blive kørt, eller en inspektion eller analyse udført for at fremlægge det krævede bevis.
tabellerne nedenfor illustrerer, hvordan det kan se ud. De viser også sporbarheden, som FDA forventer.
| produktkrav | verifikationstest | ||
|---|---|---|---|
| Prrk-0001 | ventilatoren skal have en maksimal indstilling af 2-liters volumenstyrede vejrtrækninger ved 20 vejrtrækninger pr. | TCase-0004 | Test case: kontroller maksimale åndedrætsindstillinger eller kombinationer af åndedrætsindstillinger. |
| Prrk-0002 | ventilatoren skal køre på batteristrøm ved maksimale indstillinger i mindst 90 minutter. | TCase-0005 | Test suite: Bekræft kørselstid på maksimale indstillinger med et fuldt opladet nyt batteri. |
| TCase-0006 | Test suite: Bekræft køretid på maksimale indstillinger med et batteri, der har været igennem 50 opladningscyklusser. | ||
| PRR-0003 | ventilatoren skal kunne monteres på et rullestativ. | TCase-0007 | Demonstrationstest: demonstrere, at ventilatoren kan fastgøres og løsnes fra rullestativet. |
| prrk-0004 | ventilatoren og stativet skal kunne krydse typiske tærskler for hospitalsdøre og elevatorer. | TCase-0008 | Ekstern Test: Test udført af en testtjeneste for at verificere ventilator og stativ kan rulles over en tærskel uden at vippe i henhold til IEC 60601-1 medicinsk elektrisk Standard. |
verifikation af produktkravene, som ovenfor, viser, at produktet gør, hvad vi sagde, det ville gøre.
verifikation af designspecifikationerne, som vi viser næste, viser, at produktet gør det som vi sagde, at det ville gøre det.
| designspecifikation | verifikationstest | ||
|---|---|---|---|
| DSpec-0001 | en turbine, der kan generere 40 liter luft pr.minut. | TCase-0009 | Test Suite: kontroller luftgenerering med turbine ved 40 lpm på enten vekselstrøm eller batteristrøm. |
| DSpec-0002 | en lithium-ion-batteripakke, der er klassificeret til 100 Amp-Timer. | TCase-0010 | Inspektionstest: Kontroller, at batterikøbsspecifikationen viser, at typen er lithiumion. |
| TCase-0011 | Analysetest: indsamle testdata og udføre dataanalyse for at demonstrere batteriets ydeevne i batteriets levetid vil opfylde eller overstige 100 Amp Timer. | ||
| DSpec-0003 | monteringen til rullestativet bruger en stålhåndtagsklemme, der er klassificeret til 22 lbs. | TCase-0012 | Inspektionstest: Kontroller, at delspecifikationen er for en stålhåndtagsklemme, der er klassificeret til 22 kg eller mere. |
| DSpec-0004 | stativbasen er 22″ bred med 5 hjul. |
TCase-0013 |
Test Case: Mål bunddiameter; tælle hjul; mål hjuldiameter |
| DSpec-0005 | stativhjulene har en 4″ diameter. | ||
i det væsentlige skal vi i designverifikation demonstrere, at det produkt, vi byggede, er det produkt, vi sagde, at vi ville bygge.
når den samles i en v&V-rapport, giver kombinationen af verifikations-og valideringstestresultater sammen med sporbarhed tilbage til brugerbehov, produktkrav og designspecifikationer en del af det bevis, som FDA kræver, når FDA indsender et medicinsk udstyr til godkendelse.
Validering vs Verifikationsoversigt
Her er en kort, hvis lidt forenklet, oversigt over nøgleforskelle.
|
Design Verification |
Design Validation |
|
Design output is as expected. |
Final design meets user’s needs. |
|
System, subsystem and unit testing. |
System testing. |
|
During development. |
After development. |
|
Test individual module or completed system under any conditions. |
Test conditions per user needs. |
|
inkluderer systeminspektioner, analyse og test. |
omfatter afprøvning af produktionsækvivalente enheder under reelle anvendelsesforhold. |
|
indeholder rapporter om test udført, testresultater og sporbarhed. Rapporterne gennemgås, godkendes og underskrives. |
inkluderer endelig rapport med testresultater og sporbarhed klar til lovgivningsmæssig gennemgang. Rapporterne gennemgås, godkendes og underskrives. |
Grundlæggende om Designvalideringsproces
designvalideringsprocessen vil stort set bestå af at teste enheden. Du kan udføre dette på flere måder afhængigt af omstændighederne. Aktiviteter kan omfatte:
- sammenligning med lignende udstyr, der udfører til lignende formål.
- simulering af funktionalitet gennem matematisk modellering.
- test af det endelige design for at bevise, at systemet fungerer som defineret i brugerens behov.
testplan, testcases, testkørselsregistre og testresultater skal dokumenteres og vedligeholdes som en del af designregistre. Validering er i sin helhed ikke resultatet af en enkelt aktivitet, men indsamlingen af resultater fra alle valideringsaktiviteter.
Grundlæggende om Designverifikationsproces
verifikation kan reduceres til en simpel fem-trins proces.
identificering og forberedelse
Identificer den bedste metode til gennemførelse af verifikation. Definer, hvad du vil måle, og hvordan du vil måle det. Du vil også overveje de nødvendige ressourcer, arbejdskraft og værktøjer til vellykket verifikation.
planlægning
planlægning til verifikation sker gennem hele projektets livscyklus. Du udvikler testplanen, der fanger kritiske milepæle. Planen skal opdateres, når der foretages ændringer i designindgange.
udvikling
produktudvikling begynder! Det udføres ved hjælp af den valgte metode (Scrum, vandfald, hybrid osv.). Denne del af processen inkluderer også skrivning, testkørsel og godkendelse af de testsager, der vil blive brugt til verifikation.
udførelse af
testprocedurer udføres som planlagt. Eventuelle ugyldige resultater dokumenteres og gennemgås, og enten accepteres eller logges som fejl. Fejl i produktet løses og frigives, og regressionstest udføres. Der oprettes en sporbarhedsmatrice for at kontrollere, at designinput, der er identificeret i verifikationstestplanen, er testet og bestået.
rapportering
rapportering udføres ved afslutningen af hver verifikationsfase. Detaljerede rapporter inkluderer konfigurationsstyring og frigivelsesrapporter, testresultater efter testtype eller produktversion og problemer, der blev fundet under verifikationsaktiviteten. En rapport om designverifikation af sporbarhed viser testresultater og dækning af kravene. Endelig gennemføres og godkendes anmeldelser efter hver designverifikationsaktivitet.
6 tip til bedre Validering & verifikation
Her er tip til at sikre, at du får mest muligt ud af din Validering & verifikationsaktiviteter.
Planlæg fremad (og Test tidligt)
har en solid plan på forhånd og loop alle ind. Inkluder testingeniører tidligt i udviklingsplanlægningen for at sikre, at krav og design er klare, komplette og testbare. Siger Megan, ” tidlig udvikling af testmetoder kan kaste lys over teknologiproblemer, før de bliver store hindringer.”Tidlig testudvikling kan også give testværktøjer. Disse kan derefter bruges til at fremskynde produktudviklingsprocessen samt give testbevis under formel test.
brug delt nomenklatur
at få dit team på samme side er afgørende for vellykket designvalidering& verifikation. En del af at komme på samme side betyder at bruge en delt terminologi. Brug af de samme udtryk eliminerer forvirring for teammedlemmer (ikke kun nye medlemmer — også veteraner). Se ordlisten over udtryk og almindelige akronymer nedenfor for at hjælpe med at udvikle dit fundament for terminologi.
brug værktøjer med End-to-End sporbarhed
på sin enkleste måde kan sporbarhed opnås med orddokumenter og regneark, men de genererer så meget manuelt arbejde (og er så fejlbehæftet), at du ønsker, at du startede med et dedikeret værktøj.
“en nøjagtig spormatrice er uvurderlig, når man udfører regressionsanalyse for at bestemme, hvad der skal testes igen efter en produktændring eller en fejlrettelse.”- Megan Martin, v &V konsulent
brug af et værktøj med stærke krav-til-test-til-resultater sporingskapacitet hjælper dig med at identificere huller i dækningen og give tidlige advarsler om skrøbelige eller uprøvede områder i produktet.
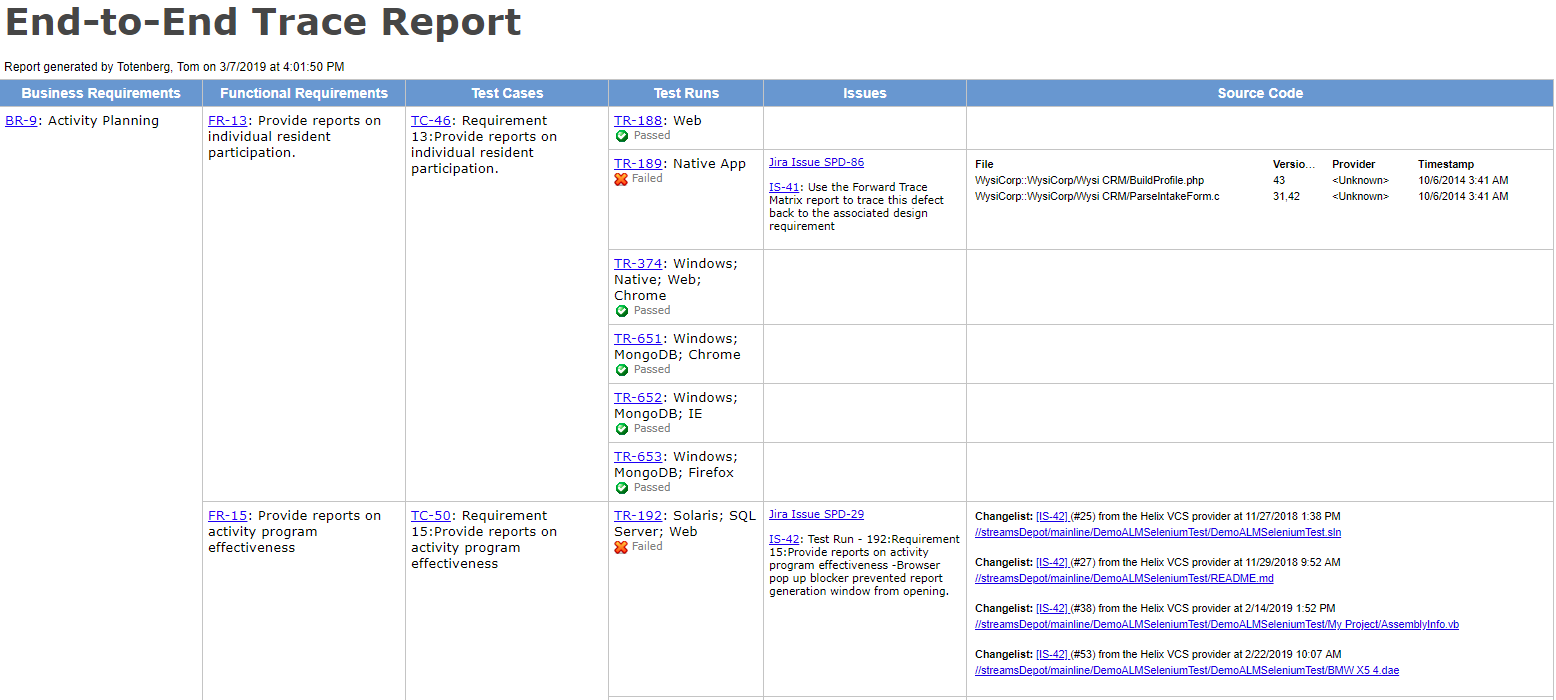
få ende-til-ende sporbarhed nu
Byg din Sporingsmatrice, mens du går
“det kan være fristende at udskyde det, men vent ikke med at opbygge din sporingsmatrice!”siger Megan. Opbygning af din sporbarhed, mens du går, forhindrer huller i at udvikle sig ubemærket. Få ting er sværere at komme sig efter end at opdage, at du har gået glip af kritiske krav, risikobegrænsende funktioner eller vigtige tests, lige når du tror, at dit udviklingsarbejde er afsluttet.
det kræver meget mindre vedligeholdelsesindsats at opretholde sporbarhed, da dine krav, design og test udvikler sig, end det gør at lappe kritiske huller i design og udvikling på den 11.time. Denne indsats kan også hjælpe dig med at identificere, hvor meget arbejde der er tilbage, hvor du muligvis skal tilføje udviklings-eller testpersonale, eller hvornår du skal revurdere leveringsplaner.
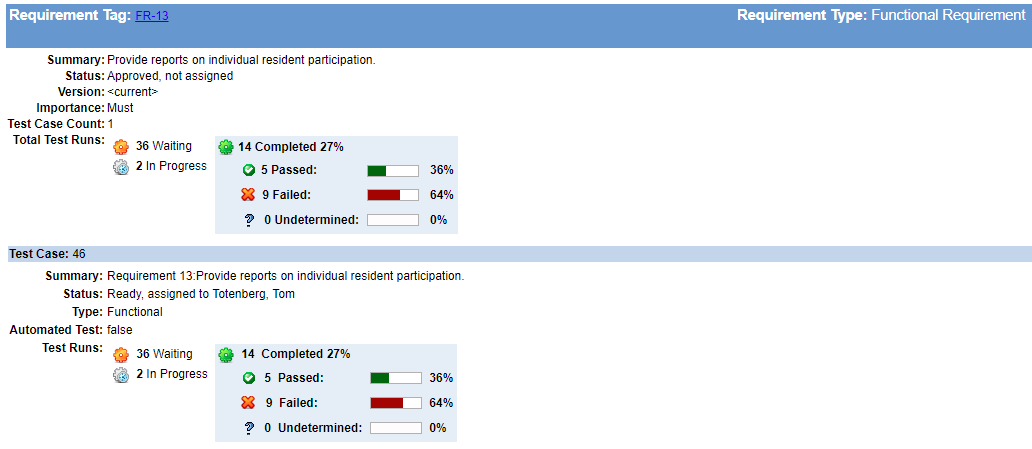
Integrer krav sporbarhed& test med anomali Tracking
at kunne linke anomalier direkte til et krav forbedrer kommunikationen mellem testere og udviklere. Det er yderst hjælpsomt. Generering af anomalier direkte fra en testprotokolfejl betyder, at flere detaljer om problemet er fanget. Som et resultat kan problemer lettere dokumenteres, gengives, rettes og testes igen.
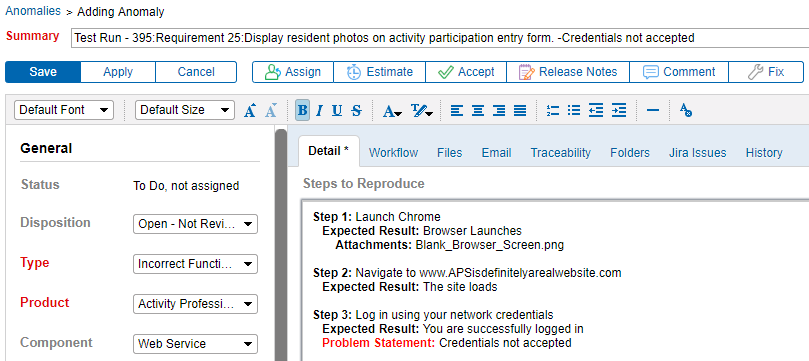
Vælg Værktøjer, du kan tilpasse til din metode
“uanset hvilken udviklingsmodel du har valgt — Agile, iterative, modificerede Vandfald — du vil vælge V&V-værktøjer, der tjener dig ved at tilpasse dig din proces i stedet for at tvinge dig til at tilpasse din proces til at betjene værktøjet,” rådgiver Megan.
de udviklingsværktøjer til medicinsk udstyr, du vælger, skal tilføje nøjagtigheden og effektiviteten af det arbejde, dit team udfører, og ikke tilføje unødvendige omkostninger til deres daglige opgaver. Et godt værktøj giver beskyttelsesskinner for at sikre, at de vigtige ting altid gøres. Det giver dit team fleksibilitet til at producere ad hoc-visninger og rapporter for bedre at bruge (og udforske) de data, du har fanget. Det giver V & V målrettet datafangst og rapportering for at gøre produktionen af rapporter enkel og gentagelig.
tag dig tid til at definere, hvordan du vil have værktøjer til at understøtte dit team, før du vælger. Få derefter dine værktøjer konfigureret til dit teams behov.
at bringe det hele sammen
designvalidering og verifikation er væsentlige komponenter i vellykket enhedsudvikling. Med fælles forståelse blandt teamet såvel som de rigtige værktøjer har du solide rammer for at få din enhed på markedet.
Se hele DEMO nu >>
forenkle V&V med spiral ALM
se, hvordan alm kan fremskynde udviklingen af medicinsk udstyr.
Udforsk spiral ALM
*igen takket være V & V ekspert Megan Martin, der gav uvurderlig indsigt til denne blog!
V& V: ordliste
faktisk resultat – hvad et system faktisk gør, når en handling udføres.
anomali – når et system ikke fungerer som forventet. For eksempel en fejl, fejl eller testfejl.
leverbar – et obligatorisk objekt produceret som et resultat af projektudførelse, normalt dokumenter i valideringsindsats.afvigelse-når en proces eller procedure ikke kan udføres som defineret, og der anvendes en alternativ metode eller materiale.
forventet resultat – hvad et system skal gøre, når en handling udføres.
integrationstest-test udført ved hjælp af to eller flere delsystemer for at verificere interaktion og indbyrdes afhængighed af delsystemerne.
protokol-en samling af testsager, der bruges til at dokumentere systemtest.
kvalifikation – en testprotokol, der angiver, at et system opfylder en defineret samling af krav.
kvalitetssikring-teammedlemmer, der har til opgave at sikre produktkvalitet eller procesintegritet.
Krav – noget et system skal kunne gøre.
retrospektiv Validering-validering af et system, der allerede eksisterer.
specifikation-et dokument, der beskriver kravene til et system eller en komponent.
Delsystemtest – test udført på et større delsystem eller en gruppe af komponenter.
System-den ting, der gennemgår Validering.
systemejer – den person, der i sidste ende er ansvarlig for et system.
systemtest-test udført ved hjælp af systemet som helhed.
Test Case – en dokumenteret procedure, der bruges til at teste, at et system opfylder et krav eller indsamling af krav.
testplan-en testmetode, der er etableret for at sikre, at et system opfylder kravene.
Testtrin – en individuel linje i en testsag. Det skal indeholde instruktioner, forventet resultat og faktisk resultat.
sporbarhed-evnen til at sikre, at kravene i specifikationerne er testet. Ofte fanget i en krav sporbarhed matrice.
enhedstest – test udført på en programmel-eller maskinenhed eller et modul på lavt niveau.
Validering-fastlæggelse ved objektiv dokumentation for, at udstyrsspecifikationer er i overensstemmelse med brugernes behov og tilsigtede anvendelse(er).
Valideringspakke-en samling af dokumenter produceret under et valideringsprojekt.
verifikation-bekræftelse ved undersøgelse og tilvejebringelse af objektiv dokumentation for, at specificerede krav er opfyldt.
V&V Plan – en plan, der definerer de krav, der skal verificeres og valideres, og arbejdskraften, ansvarlige personer, værktøjer, metoder, ressourcer og tidsplan for V&V indsats.
fælles Designvalidering akronymer
CC – Change Control
CCB – Change Control Board (en gruppe af personer, der kontrollerer, hvilke ændringer der foretages, og hvornår)
DS – designspecifikation
FAT – Factory Acceptance Test
FS – funktionel specifikation
FRS – funktionel Kravspecifikation (se funktionel specifikation)
GCP – god klinisk praksis (kvalitetsretningslinjer for kliniske operationer)
GLP – god laboratoriepraksis (kvalitetsretningslinjer for farmaceutiske laboratorie operationer)
GMP – god fremstilling P>
SAD – Programarkitekturdokument eller Systemarkitekturdokument
Test af accept af SAT – site
SCCB – Programændringskontrolkort (samme som CCB, men for programmer)
SDD – Programdetaljedesigndokument
SDS – Programdesignspecifikation
Spec – specifikation
SRS – krav specifikation
TM – sporbarhedsmatrice
UAT – test af brugeraccept
Urs – brugerkrav Specification
UUT – Unit Under Test
VMP – Validation Master Plan
VP – Validation Plan
V&V – Verification and Validation