Einleitung
Verlängerte Lungenluftlecks sind häufig und können zu einem hohen Maß an Morbidität, längeren Krankenhausaufenthalten, infektiösen und kardiopulmonalen Komplikationen führen.1,2
Obwohl es Unterschiede zwischen den verschiedenen Autoren in ihrer Definition von Luftlecks gibt, haben neuere Studien zur Lungenlobektomie eine ungefähre durchschnittliche Dauer des Krankenhausaufenthalts von 5 Tagen festgestellt; und so wurde vorgeschlagen, dass ein anhaltendes Luftleck als ein Luftleck definiert werden sollte, das über den postoperativen fünften Tag hinaus anhält.3 In der Tat steht dies im Einklang mit der Datenbankdefinition der Society of Thoracic Surgeons, die sich auf anhaltende Luftlecks als solche bezieht, die typischerweise auftreten, wenn der Patient andernfalls entlassen würde, wenn nicht das anhaltende Luftleck vorhanden wäre.
Die überwiegende Mehrheit der postoperativen Luftlecks sind alveoläre Luftlecks; Dies ist relevant, da sich deren Behandlung stark von der Behandlung von bronchopleuralen Fisteln unterscheidet, die häufig einen sofortigen chirurgischen Eingriff erfordern.3
Der am konsistentesten identifizierte Risikofaktor für ein längeres Luftleck ist eine chronisch obstruktive Lungenerkrankung,4 ein niedriges erzwungenes Exspirationsvolumen in der 1. Sekunde und ein niedriger maximaler freiwilliger Beatmungsprozentsatz.5,6
Zu den Behandlungsmöglichkeiten längerer Luftlecks gehören ein wachsames Warten mit kontinuierlicher Drainage durch eine Thorakostomiesonde,6 Pleurodese, chirurgische Eingriffe,2 sowie der Einsatz endoskopischer Techniken.
Endobronchiale Ansätze umfassen die Anwendung von Gelschaum, die Verwendung von Fibrinkleber, Spulen oder Endobronchialklappen.1,7 Im Allgemeinen wird das Aufblasen eines Ballonkatheters verwendet, um die segmentalen oder subsegmentalen Atemwege zu identifizieren, die für das Luftleck verantwortlich sind.8 Schweigert et al.9 berichtete über eine andere Methode unter Verwendung von Methylenblau über die Thoraxschläuche. Wir beschreiben einen Fall eines anhaltenden Luftlecks, das mit Endobronchialventilen behandelt wurde Platzierung in Segmenten, die mit Methylenblau über den Thoraxschlauch identifiziert wurden.
Fallbericht
Ein 68-jähriger Mann zeigte Husten, Gewichtsverlust und eine Lungenmasse im rechten Mittellappen (ML).
Er war Ex-Raucher mit einer 450-jährigen Rauchgeschichte und war während seines Berufslebens viele Jahre Asbest ausgesetzt gewesen. Seine frühere Krankengeschichte beinhaltete eine Prostatektomie aufgrund von Prostatakrebs 6 Jahre zuvor ohne Anzeichen eines erneuten Auftretens.
Ein pulmonales Adenokarzinom wurde durch transthorakale Nadelaspirationsbiopsie der ML–Läsion diagnostiziert und die Positronen-Emissions-Tomographie-Computertomographie (PET/ CT) -Scan für das Staging durchgeführt, ergab Fluorodesoxyglucose (FDG) Aufnahme nicht nur auf der ML-Masse (maximaler standardisierter Aufnahmewert (SUVmax) -11), sondern auch auf der rechten Pleura, was zu weiteren Pleurauntersuchungen mit mehreren Biopsien führte, die für maligne Zellen negativ waren. Er wurde T2N0M0 inszeniert und operiert
Eine Thorakotomie mit einer rechten Mittellobektomie, die eine Teilung des dreieckigen Ligaments sowie eine systematische Lymphadenektomie beinhaltete, wurde durchgeführt, und da während des Eingriffs Pleuraplaques gefunden wurden, wurden sie entfernt und eine Pleuradekortikation des unteren rechten Lappens durchgeführt.Die Pathologie bestätigte ein pT1bN0R0-Adenokarzinom ohne Anzeichen einer malignen Pleurabeteiligung, aber es wurde auch eine chronische fibrinöse Pleuritis diagnostiziert.
Die Extubation des Patienten war kurz nach der Operation möglich und eine postoperative mechanische Beatmung war nicht erforderlich. Die Kinesiotherapie, eine routinemäßige und weithin anerkannte Intervention zur Verbesserung der Lungenexpansion, wurde so schnell wie möglich begonnen.Obwohl die Lungenexpansion innerhalb von 2 Tagen erreicht wurde, wurde ein Luftleck festgestellt und die zur Aufrechterhaltung der Lungenexpansion erforderliche Absaugung wurde für weitere zehn Tage fortgesetzt, bis während der normalen Gezeitenatmung kein sichtbares Luftleck mehr auftrat. Zu diesem Zeitpunkt wurde die Absaugung gestoppt und die Schläuche nach 2 Tagen geklemmt. Da kein klinischer Kompromiss, kein sich verschlechternder Pneumothorax oder eine Zunahme der subkutanen Luft auftrat, wurde der Thoraxschlauch entfernt (Abb. 1), und der Patient wurde innerhalb von 48 Stunden aus dem Krankenhaus entlassen.
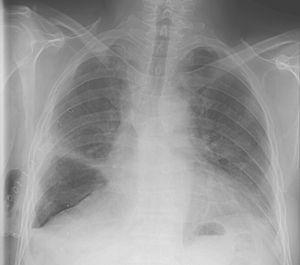
Thoraxröntgenaufnahme am 12.Tag nach rechter Mittelohrlobektomie und 24h nach Thoraxröhrenremotion.
Zwei Wochen nach der Entlassung aus dem Krankenhaus – 1 Monat nach der Operation – wurde er mit den klinischen Symptomen einer Brustinfektion wieder aufgenommen. Ein Thorax-CT-Scan zeigte einen rechten großen vorderen Hidropneumothorax, Pleuradicke und subkutanes Emphysem. Ein Empyem und ein postoperatives Luftleck wurden diagnostiziert. Großspektrum-Antibiotika wurden eingeleitet, ein Thoraxschlauch wurde sofort eingesetzt und eine Bronchofibroskopie verwendet, um die Stumpfintegrität und das Fehlen anderer endobronchialer Komplikationen zu beurteilen. Trotz dieser Maßnahmen unterzog sich der Patient einer pleuro-pulmonalen Dekortikation, die durch dichte Pleuraadhäsionen kompliziert wurde. Während des Eingriffs wurde eine Naht von Lungenrissen durchgeführt und Tissucol® Spray verwendet, um die Luftlecks zu kontrollieren. Obwohl sich der klinische Gesundheitszustand und die Infektionsparameter anfänglich verbesserten, hatte der Patient ein anhaltendes Luftleck mit einem stabilen asymptomatischen Pneumothorax auf der Wasserdichtung, das zunahm, wenn die negative Absaugung ausgesetzt wurde und der Brustabfluss in freier Drainage belassen wurde.
Während dieser Zeit wurde ein wachsames Warten mit kontinuierlicher Drainage durch einen Thoraxschlauch für 2 Monate aufrechterhalten, bis das Luftleck gelöst zu sein schien und der Patient es tolerieren konnte, dass der Drain eingeklemmt wurde; Eine Talk-Pleurodese durch den Thoraxschlauch wurde ohne zufriedenstellende Ergebnisse versucht.
Zur Kontrolle des Luftlecks wurde ein endoskopischer Ansatz ausprobiert. Ein durch das Bronchoskop eingeführter Ballonkatheter wurde auf verschiedene Segmente aufgeblasen, während die Beobachtung des Thoraxdrainagesystems das Luftleck bewertete. Eine Verringerung des Luftlecks schien erreicht zu werden, wenn B7- und B8-Segmente des unteren rechten Lappens verschlossen und Ventile (Zephyr EBV) in diesen Segmenten platziert wurden. Die Endobronchialklappen wurden mit einem flexiblen Katheter in Position gebracht. Die Ventile wurden unter Verwendung eines mit dem System gelieferten Ventilladers in die distale Spitze des Abgabekatheters komprimiert. Der Abgabekatheter wurde dann durch den Arbeitskanal eines Standardbronchoskops für Erwachsene (> 2,8 mm Innendurchmesser) geführt und zu den Zielluftwegen geführt. Einmal an Ort und Stelle wurde das Ventil eingesetzt. Dadurch wurde jedoch nur eine Verringerung des Luftlecks erreicht.
Drei Wochen später (4 Monate nach der ersten Operation) wurde eine Thorakomyoplastik mit einem Rectus abdominis-Lappen durchgeführt, um den Pleuraraum auszulöschen, und die Endobronchialklappen wurden entfernt. Drei Wochen nach dieser späteren Operation war es möglich, den Thoraxschlauch ohne klinische oder radiologische Verschlechterung zu klemmen und zu entfernen.
Leider wurde der Patient zwei Wochen später mit Atemnot und einem Pneumothorax wieder aufgenommen, so dass ein Thoraxschlauch zurückgelegt und abgesaugt wurde (Abb. 2). Der Patient war klinisch nicht für eine Operation geeignet, daher wurde erneut ein endoskopischer Ansatz versucht.

Thorax-CT-Scan zeigt Pleurahöhle mit einem Thoraxschlauch im Inneren und Pleuraverdickung.
Dieses Mal wurde die Instillation von Methylenblau (1 Ampulle verdünnt in 1 Liter Kochsalzlösung) über den Thoraxschlauch verwendet, um das zur Fistel führende Bronchialsegment zu lokalisieren. Während die blaue Lösung eingeflößt wurde, schaute ein anderer Kliniker durch das Bronchoskop und beobachtete, wie die blaue Lösung auf den Segmenten erschien, die zur Fistel führten. Die Segmente B6 und B7 wurden visuell identifiziert (Abb. 3) und Endobronchialklappen wurden wie oben beschrieben eingesetzt.
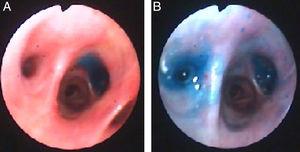
Methylenblau auf Segment B7 (Panel A) und B6 (Panel B) des rechten Unterlappens nach Instillation durch den Thoraxschlauch.
Nach dem Eingriff schien die Größe des Luftlecks verringert zu sein und es wurde versucht, es zu klemmen. Da es keine Hinweise auf eine Verschlechterung des Pneumothorax, eine fortschreitende subkutane Luftentwicklung oder Dyspnoe gab, wurde der Thoraxschlauch entfernt.
Der Gesundheitszustand des Patienten verbesserte sich langsam und er wurde aus dem Krankenhaus entlassen. Bei der Nachuntersuchung wurden Metastasen in beiden Lungen gefunden und der Patient starb 8 Monate später.
Diskussion
Die Autoren beschreiben einen Fall eines anhaltenden Luftlecks nach Lungenresektion. Luftlecks sind ein häufiges Problem, das häufig mit längeren Krankenhausaufenthalten, infektiösen und kardiopulmonalen Komplikationen verbunden ist und gelegentlich eine erneute Operation erfordert3 und / oder bronchoskopische Techniken.
Der vorgestellte Patient hatte mehrere Risikofaktoren für die Entwicklung eines Luftlecks, da er eine chronisch obstruktive Lungenerkrankung hatte,10 und in diesem Fall von besonderer Relevanz das Vorhandensein signifikanter Pleuraadhäsionen.5,11 Es ist sehr wahrscheinlich, dass die Pleuraadhäsionen mit seiner bekannten Asbestexposition im Erwachsenenalter zusammenhängen.
Zu den Behandlungsmöglichkeiten von Luftlecks gehören wachsames Warten, chirurgische Eingriffe sowie medizinische Therapien wie Pleurodese und insbesondere der Einsatz verschiedener Bronchoskopie-Techniken wie Leime, Coils und Dichtstoffe. Der Erfolg war variabel und es scheint keine optimale Therapie zu geben. Die derzeit möglichen Interventionen scheinen komplementär zu sein und die Behandlung sollte individualisiert werden.7 Es gibt keine kontrollierten Studien, in denen die verschiedenen Ansätze verglichen werden.
Im vorliegenden Fall war die erste Option ein chirurgischer Eingriff, da eine Thorakotomie erforderlich war, um eine Infektion zu kontrollieren, die nicht auf Antibiotika ansprach, und um durch den Thoraxschlauch zu entwässern. Während der Operation wurde versucht, die Stelle des Luftlecks zu schließen, und Tissucol® Spray wurde verwendet, aber es blieb auch nach einer Wartezeit von mehreren Wochen bestehen.
Anschließend wurde eine chemische Pleurodese versucht. Die Instillation eines Sklerosierungsmittels in den Pleuraraum durch den Thorakostomietubus fördert die Pleurasymphyse, was zu einem Leckverschluss führen kann,12 aber wie in der Literatur gezeigt, war nicht sehr effektiv.
Das Vorhandensein eines postoperativen Empyems, bei dem die Dekortikation versagt hat, und das Vorhandensein von Bronchialfisteln gelten derzeit als Indikationen für thorakomyoplastische Verfahren.13 Es ermöglicht eine vollständige und endgültige Obliteration des infizierten Pleuraraums durch eine Kombination aus Thorakoplastik und Verwendung benachbarter Muskellappen (Latissimus dorsi, Serratus anterior, pectoralis, Rectus abdominis usw.).
Dies geschah in diesem Fall, aber obwohl neuere Veröffentlichungen eine Gesamterfolgsrate von 90% zeigen, mit einer schnellen und endgültigen Heilung, war es nur wirksam bei der Kontrolle der Infektion, nicht der Fistel.
Bronchoskopische Ansätze zur Behandlung von Lungenluftlecks sind nicht nur als diagnostische, sondern auch als therapeutische Instrumente populärer geworden.
Um eine Fistel mit bronchoskopischen Techniken erfolgreich zu behandeln, muss die Fistel direkt sichtbar gemacht werden (proximale Fisteln) und es sollte Hinweise darauf geben, dass die Okklusion signifikant abgenommen hat oder das Luftleck gestoppt wurde. Die am häufigsten verwendete Technik zur Lokalisierung des Bronchialsegments, das zu den distalen Fisteln führt, ist die Verwendung von Ballons, wie Swan-Ganz-Katheter, um die Bronchialsegmente systematisch zu verschließen8 bei gleichzeitiger Beobachtung des Thoraxdrainagesystems zur Beurteilung des Luftlecks. Diese Methode kann sich bei Patienten mit kleinen Luftlecks als schwierig erweisen, die nur beim Husten und nicht bei normaler Atemzugsatmung auftreten.
Obwohl Methylenblau seit vielen Jahren zur Diagnose des Vorhandenseins von Fisteln durch Instillation durch den Stumpf verwendet wird und bei Erkennung im Thoraxschlauch eine brochopleurale Fistel bestätigen kann, wurde seine Verwendung zur Lokalisierung des zur Fistel führenden Bronchialsegments erst 2011 beschrieben.9 Methylenblau wurde über den Thoraxschlauch und unmittelbar nach der Instillation verwendet, wenn eine Fistel vorhanden war; das Methylenblau konnte vom Bronchoskopiker auf dem zur Fistel führenden Bronchialsegment gesehen werden.
Bei unserem Patienten ermöglichte die Verwendung von Methylenblau die Identifizierung von zwei Bronchialsegmenten, die an dem Luftleck beteiligt waren, eines, das dem durch die Ballonmethode identifizierten gemeinsam ist, aber auch eines, das durch die vorherige Technik nicht vermutet wurde.
Nach der Identifizierung des Bronchialsegments können mehrere Ansätze in Betracht gezogen werden, darunter die Anwendung von Gelfoam, die Verwendung von Fibrinkleber, die Platzierung von Spulen, Stents und Endobronchialklappen.7 Es gibt keine kontrollierten Studien, um festzustellen, welche davon am effektivsten oder sichersten ist. Travaline et al.1 zeigte, dass die Implantation von endobronchialen Einwegventilen (Zephyr EBV) bei einer großen Anzahl von Patienten mit längeren Luftlecks wirksam war. Bei 48% der Patienten wurde eine vollständige Beendigung des Luftlecks und bei 45% eine Verringerung des Ausmaßes erreicht.
In diesem Fall verringerte die Implantation einer Zephyrklappe auf den Segmenten B6 und B7 in Verbindung mit Pleuraheilung und Verdickung die Größe des Luftlecks so weit, dass der Thoraxschlauch entfernt werden konnte. Diese nicht-chirurgischen Ansätze erscheinen vielversprechend und können für einige Patienten die einzige Behandlungsoption sein. Die Autoren möchten die Verwendung von Methylenblau über den Thoraxschlauch hervorheben, um die Segmente des anhaltenden Luftlecks zu identifizieren und die Platzierung der Endobronchialklappen zu steuern.
Ethische Angaben
Schutz von Menschen und Tieren. Die Autoren erklären, dass für diese Studie keine Experimente an Menschen oder Tieren durchgeführt wurden.
Vertraulichkeit der Daten. Die Autoren erklären, dass sie die Protokolle ihres Arbeitszentrums zur Veröffentlichung von Patientendaten befolgt haben und dass alle in die Studie einbezogenen Patienten ausreichende Informationen erhalten und ihre schriftliche Einwilligung zur Teilnahme an der Studie erteilt haben.