Forma de dosificación: Inyección
Revisado médicamente por Drugs.com. Última actualización el 22 de mayo de 2020.
- Overview
- Side Effects
- Dosage
- Professional
- Interactions
- More
FOR USE IN NERVE AGENT POISONING ONLY
A Sterile Solution For Intramuscular Use Only
Rx Only
- Pralidoxime Chloride Description
- Cloruro de pralidoxima – Farmacología clínica
- Indicaciones y uso para Cloruro de Pralidoxima
- Contraindicaciones
- Advertencias
- Precauciones
- General:
- Información para los pacientes:
- Pruebas de laboratorio:
- Interacciones medicamentosas:
- Carcinogénesis, Mutagenia, Deterioro de la Fertilidad:
- Embarazo
- Madre Lactante:
- Uso pediátrico:
- Reacciones adversas
- Abuso y dependencia de drogas
- Sobredosis
- Manifestaciones de sobredosis:
- Tratamiento de la sobredosis:
- Acute Toxicity:
- Dosis y Administración de cloruro de Pralidoxima
- Instrucciones de Uso:
- Cómo se suministra el cloruro de Pralidoxima
- Panel de visualización Principal – Inyección de cloruro de Pralidoxima, Etiqueta de 300 mg
- More about pralidoxime
- Recursos para el consumidor
- Recursos profesionales
- Guías de tratamiento relacionadas
Pralidoxime Chloride Description
Pralidoxime Chloride Injection (auto-injector) provides Pralidoxime Chloride in a sterile solution for intramuscular injection.
Cada autoinyector precargado proporciona una dosis del antídoto, cloruro de pralidoxima, en una unidad autónoma, diseñada especialmente para la autoadministración automática o en pareja por personal militar. Pralidoxima en el autoinyector también puede ser administrada por personal civil cualificado de respuesta a emergencias que haya recibido la formación adecuada en el reconocimiento y tratamiento in situ de la intoxicación por agentes nerviosos en caso de liberación accidental de agentes nerviosos. El procedimiento recomendado (ver DOSIFICACIÓN Y ADMINISTRACIÓN) es inyectar el contenido del autoinyector en los músculos de un muslo externo.
Después de activar un autoinyector, el recipiente vacío debe desecharse adecuadamente (ver DOSIFICACIÓN Y ADMINISTRACIÓN), no se puede rellenar ni se puede retraer la aguja que sobresale.
Cuando se activa, cada autoinyector dispensa 600 mg de cloruro de Pralidoxima en 2 ml de una solución estéril que contiene 20 mg/ml de alcohol bencílico, 11,26 mg/ml de glicina en Agua para inyección, USP. El pH se ajusta con ácido clorhídrico. El rango de pH es de 2,0 a 3,0. El producto no contiene pirógenos.
El cloruro de pralidoxima es un reactivador de la colinesterasa.
Nombre Químico: cloruro de 2-formil-1 metilpiridinio oxima (metocloruro de piridina-2-aldoxima). También conocido como cloruro de 2-PAM.
Fórmula estructural:
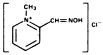
El cloruro de pralidoxima se presenta como un polvo cristalino inodoro, blanco, no higroscópico, soluble en agua en la medida de 1 g en menos de 1 ml. Estable en el aire, se funde entre 215 ° C y 225°C, con descomposición.
La actividad específica del fármaco reside en el ion metilpiridinio 2-formil-1 y es independiente de la sal particular empleada. El cloruro es preferido debido a su compatibilidad fisiológica, excelente solubilidad en agua a todas las temperaturas y alta potencia por gramo, debido a su bajo peso molecular (173).
Cloruro de pralidoxima – Farmacología clínica
El cloruro de pralidoxima es un reactivador de la colinesterasa.
La acción principal de la pralidoxima es reactivar la colinesterasa (principalmente fuera del sistema nervioso central) que ha sido inactivada por fosforilación debido a un plaguicida organofosforado o compuesto relacionado. La destrucción de la acetilcolina acumulada puede proceder y las uniones neuromusculares volverán a funcionar normalmente. La pralidoxima también retrasa el proceso de «envejecimiento» de la colinesterasa fosforilada a una forma no reactivable, y desintoxica ciertos organofosfatos por reacción química directa. El medicamento tiene su efecto más crítico para aliviar la parálisis de los músculos de la respiración. Debido a que la pralidoxima es menos eficaz para aliviar la depresión del centro respiratorio, siempre se requiere atropina de forma concomitante para bloquear el efecto de la acetilcolina acumulada en este sitio. La pralidoxima alivia los signos y síntomas muscarínicos, la salivación, el broncoespasmo, etc., pero esta acción es relativamente poco importante ya que la atropina es adecuada para este propósito.
La pralidoxima se distribuye por el agua extracelular, no se une a las proteínas plasmáticas. El fármaco se excreta rápidamente en la orina, en parte sin cambios, y en parte como un metabolito producido por el hígado. En consecuencia, la pralidoxima es de acción relativamente corta y pueden ser necesarias dosis repetidas, especialmente cuando hay evidencia de absorción continua del veneno.
La concentración terapéutica mínima de pralidoxima en plasma es de 4 µg / ml, este nivel se alcanza en aproximadamente 16 minutos después de una inyección única de cloruro de pralidoxima de 600 mg. La semivida aparente del cloruro de pralidoxima es de 74-77 minutos.
Se ha notificado que el uso complementario de reactivadores de la colinesterasa de oxima (como la pralidoxima) reduce la incidencia y la gravedad de los defectos del desarrollo en embriones de pollo expuestos a teratógenos conocidos como paratión, bidrina, carbacol y neostigmina. Se demostró que este efecto protector de las oximas estaba relacionado con la dosis.
Indicaciones y uso para Cloruro de Pralidoxima
Este autoinyector para cloruro de Pralidoxima está específicamente indicado para uso intramuscular como complemento de la atropina en el tratamiento de intoxicaciones por agentes nerviosos con actividad anticolinesterasa.
Contraindicaciones
El autoinyector de cloruro de Pralidoxima está contraindicado en pacientes hipersensibles a cualquier componente del producto.
Advertencias
La pralidoxima no es eficaz en el tratamiento de intoxicaciones debidas a fósforo, fosfatos inorgánicos u organofosfatos que no tienen actividad anticolinesterasa.
Precauciones
General:
La pralidoxima ha sido muy bien tolerada en la mayoría de los casos, pero debe recordarse que la condición desesperada del paciente envenenado con organofosforados generalmente enmascara los signos y síntomas menores que se han observado en sujetos normales.
Debido a que la pralidoxima se excreta en la orina, una disminución de la función renal dará lugar a un aumento de los niveles sanguíneos del medicamento. Por lo tanto, la dosis de pralidoxima debe reducirse en presencia de insuficiencia renal.
Información para los pacientes:
El autoinyector de cloruro de Pralidoxima debe ser autoadministrado por personal militar o administrado por personal civil cualificado de respuesta a emergencias solo después de que se hayan producido los siguientes acontecimientos:
– el individuo se ha puesto la máscara después de reconocer la existencia de un peligro de agente químico en su área – algunos o todos los síntomas de envenenamiento por agente nervioso que se citan a continuación están presentes: congestión nasal inexplicable en el pecho con dificultad para respirar pupilas localizadas del ojo que producen visión borrosa babeo, sudoración excesiva náuseas, vómitos y calambres abdominales micción y defecación involuntarias espasmos, espasmos y dolor de cabeza asombroso, somnolencia, coma, convulsiones interrupción de la respiración
Se deben tomar las medidas adecuadas para asegurar que el personal equipado con autoinyectores comprenda sus indicaciones y uso, incluida la revisión de los síntomas de intoxicación y el funcionamiento del autoinyector.
Pruebas de laboratorio:
El tratamiento de la intoxicación por organofosforados se debe instituir sin esperar los resultados de las pruebas de laboratorio. Las mediciones de glóbulos rojos, colinesterasa plasmática y paranitrofenol urinario (en el caso de exposición al paratión) pueden ser útiles para confirmar el diagnóstico y seguir el curso de la enfermedad. Se ha observado una reducción en la concentración de colinesterasa de glóbulos rojos por debajo del 50% de lo normal solo con intoxicación por ésteres organofosforados.
Interacciones medicamentosas:
Cuando la atropina y la pralidoxima se usan juntas, los signos de atropinización (rubor, midriasis, taquicardia, sequedad de boca y nariz) pueden aparecer antes de lo esperado cuando la atropina se usa sola. Esto es especialmente cierto si la dosis total de atropina ha sido grande y la administración de pralidoxima se ha retrasado.2, 3, 4
Las siguientes precauciones deben tenerse en cuenta en el tratamiento de anticholesterinase intoxicación, aunque no influyen directamente en el uso de pralidoxime; dado que los barbitúricos son potenciados por las anticolinesterasas, se deben usar con precaución en el tratamiento de convulsiones; se deben evitar la morfina, la teofilina, la aminofilina, la succinilcolina, el pino reser y los tranquilizantes de tipo fenotiacina en pacientes con intoxicación por organofosfatos.
Carcinogénesis, Mutagenia, Deterioro de la Fertilidad:
Dado que el autoinyector de cloruro de Pralidoxima está indicado únicamente para uso de emergencia a corto plazo, el fabricante no ha realizado investigaciones de su potencial de carcinogénesis, mutagénesis o deterioro de la fertilidad, ni se ha informado de ellas en la bibliografía.
Embarazo
No se han realizado estudios de reproducción en animales con pralidoxima. Tampoco se sabe si la pralidoxima puede causar daño fetal cuando se administra a una mujer embarazada o puede afectar la capacidad de reproducción. La pralidoxima se debe administrar a una mujer embarazada solo si es claramente necesario.
Madre Lactante:
No se sabe si este medicamento se excreta en la leche materna. Debido a que muchos medicamentos se excretan en la leche materna, se debe tener precaución cuando se administre pralidoxima a una mujer lactante.
Uso pediátrico:
No se ha establecido la seguridad y eficacia en niños.
Reacciones adversas
Cuarenta a 60 minutos después de la inyección intramuscular, se puede experimentar dolor de leve a moderado en el lugar de la inyección.
La pralidoxima puede causar visión borrosa, diplopía y alteración de la acomodación, mareos, dolor de cabeza, somnolencia, náuseas, taquicardia, aumento de la presión arterial sistólica y diastólica, hiperventilación y debilidad muscular cuando se administra por vía parenteral a voluntarios normales que no han estado expuestos a venenos anticolinesterásicos. En los pacientes es muy difícil diferenciar los efectos tóxicos producidos por la atropina o los compuestos organofosforados de los del fármaco.
Se observaron aumentos de los niveles de enzimas SGOT y/o SGPT en 1 de 6 voluntarios sanos a los que se administró 1.200 mg de cloruro de Pralidoxima por vía intramuscular, y en 4 de 6 voluntarios a los que se administró 1.800 mg por vía intramuscular. Los niveles volvieron a la normalidad en aproximadamente 2 semanas. Se observaron aumentos transitorios de la creatinfosfoquinasa en todos los voluntarios sanos que recibieron el fármaco. Una única inyección intramuscular de 330 mg en 1 ml en conejos causó mionecrosis, inflamación y hemorragia.
Cuando la atropina y la pralidoxima se usan juntas, los signos de atropinización pueden ocurrir antes de lo esperado cuando la atropina se usa sola. Esto es especialmente cierto si la dosis total de atropina ha sido grande y la administración de pralidoxima se ha retrasado.2, 3, 4 La excitación y el comportamiento maníaco inmediatamente después de la recuperación de la conciencia se han reportado en varios casos. Sin embargo, se ha presentado un comportamiento similar en casos de intoxicación por organofosfatos que no se trataron con pralidoxima.3, 5, 6
Abuso y dependencia de drogas
El cloruro de pralidoxima no está sujeto a abuso y no posee un potencial conocido de dependencia.
Sobredosis
Manifestaciones de sobredosis:
Observadas solo en sujetos normales: mareos, visión borrosa, diplopía, dolor de cabeza, alteración de la acomodación, náuseas, taquicardia leve. En terapia, ha sido difícil diferenciar los efectos secundarios debidos al medicamento de los debidos a los efectos del veneno.
Tratamiento de la sobredosis:
Se debe administrar respiración artificial y otra terapia de apoyo según sea necesario.
Acute Toxicity:
i.v.—man TDLo: 14 mg/kg (toxic effects: CNS) i.v.— rat LD50: 96 mg/kg i.m.—rat LD50: 150 mg/kg oral—mouse LD50: 4100 mg/kg i.p.—mouse LD50: 155 mg/kg i.v.—mouse LD50: 90 mg/kg i.m.—mouse LD50: 180 mg/kg i.v.—rabbit LD50: 95 mg/kg i.m.—guinea pig LD50: 168 mg/kg
Dosis y Administración de cloruro de Pralidoxima
Exposición a agentes nerviosos que posean actividad anticolinesterasa (tipo organofosforado)
CASO LEVE: dolor de cabeza, visión borrosa, signos muscarínicos leves
CASO moderadamente GRAVE: sudoración excesiva, lagrimeo, salivación, diarrea, opresión en el pecho
Para una reactivación óptima de la colinesterasa inhibida por organofosforados, atropina y pralidoxima debe administrarse lo antes posible después de la exposición. Dependiendo de la gravedad de los síntomas, administrar inmediatamente un autoinyector que contenga atropina, seguido de un autoinyector que contenga pralidoxima. Primero se debe administrar atropina hasta que se manifiesten sus efectos y sólo entonces se debe administrar pralidoxima. Si los síntomas del agente nervioso siguen presentes después de 15 minutos, repita las inyecciones. Si los síntomas persisten después de 15 minutos adicionales, repita las inyecciones por tercera vez. Si después de la tercera serie de inyecciones, los síntomas persisten, no administre más antídotos, sino busque ayuda médica.
Instrucciones de Uso:
Cuando, como se describió anteriormente, se indique el uso del autoinyector, proceda de la siguiente manera:
|
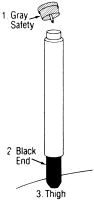 |
Cianosis DE CASO MUY GRAVE, Vergüenza respiratoria, Coma
Las medidas iniciales deben incluir la eliminación de secreciones, el mantenimiento de una vía aérea permeable y, si es necesario, ventilación artificial. La atropina no debe utilizarse hasta que se haya superado la cianosis, ya que la atropina produce fibrilación ventricular en presencia de hipoxia. La morfina, la teofilina, la aminofilina o la sucincilcolina están contraindicadas. Deben evitarse los tranquilizantes del tipo reserpina o fenotiazina.
» La pralidoxima es más eficaz si se administra inmediatamente después de la intoxicación. En general, poco se logra si el medicamento se administra más de 36 horas después de la terminación de la exposición. Sin embargo, cuando se ha ingerido el veneno, la exposición puede continuar durante algún tiempo debido a la absorción lenta de la parte inferior del intestino, y se han notificado recaídas mortales después de la mejoría inicial. La administración continuada durante varios días puede ser útil en estos pacientes. Se recomienda una estrecha supervisión del paciente durante al menos 48 a 72 horas. Si se ha producido una exposición cutánea, se debe quitar la ropa y lavar bien el cabello y la piel con bicarbonato de sodio o alcohol lo antes posible. El diazepam se puede administrar con precaución si las convulsiones no se controlan con atropina.»7
IMPORTANTE: LOS MÉDICOS Y / U OTRO PERSONAL MÉDICO QUE AYUDE A LAS VÍCTIMAS EVACUADAS DE AGENTES NERVIOSOS, DEBEN EVITAR EXPONERSE A LA CONTAMINACIÓN POR LA ROPA DE LAS VÍCTIMAS.
Cómo se suministra el cloruro de Pralidoxima
El cloruro de pralidoxima se suministra en solución acuosa prellenada en el autoinyector (600 mg, 2 ml) para uso militar y para uso de personal civil cualificado de respuesta a emergencias. Los autoinyectores se suministran a través de la Dirección de Material Médico, el Centro de Suministros de Defensa de Filadelfia u otra agencia local, estatal o federal análoga.
Cuando se activa, cada autoinyector dispensa 600 mg de cloruro de Pralidoxima en 2 ml de una solución estéril que contiene 20 mg/ml de alcohol bencílico, 11,26 mg/ml de glicina en Agua para inyección, USP. El pH se ajusta con ácido clorhídrico. El pH es de 2.0-3.0 El producto no contiene pirógenos.
Almacenar a 25 ° C (77°F); Se permiten excursiones a 15-30°C (59-86°F).Evitar la congelación.
Meridian Medical Technologies, Inc.
Columbia, MD 21046
A Pfizer Company
00001976
08/16
Impreso en EE.UU.
- Landauer, W.: Tetrógenos colinomiméticos. V. El efecto de las oximas y los reactivadores de colinesterasa relacionados, Teratología 15: 33 (Feb.) 1977.
- Moller, K. O., Jenson-Holm, J., and Lausen, H. H.: Ugeskr. Laeg.123:501, 1961.
- Namba, T., Nolte, C. T., Jackrel, Jr., y Grob, D.: Envenenamiento por insecticidas organofosforados. Manifestaciones agudas y crónicas, Amer. J. Med. 50: 475 (Abr.) 1971.
- Arena, J. M.: Envenenamiento. Toxicología. Síntoma. Tratamientos, ed. 4, Springfield, Enfermo., Charles C. Thomas, 1979, pág. 133.
- Brachfeld, J., y Zavon, M. R.: Intoxicación por fosfato orgánico (Phosdrin®). Reporte de caso y resultados del tratamiento con 2-PAM, Arch. Environ. Salud 11:859,1965.
- Hayes, W. J., Jr.: Toxicology of Pesticides, Baltimore, The Williams & Wilkins Company, 1975, p. 416.Departamento de Medicamentos de AMA: Evaluaciones de Medicamentos de AMA, ed. 4, Chicago, American Medical Association, 1980, pág. 1455.
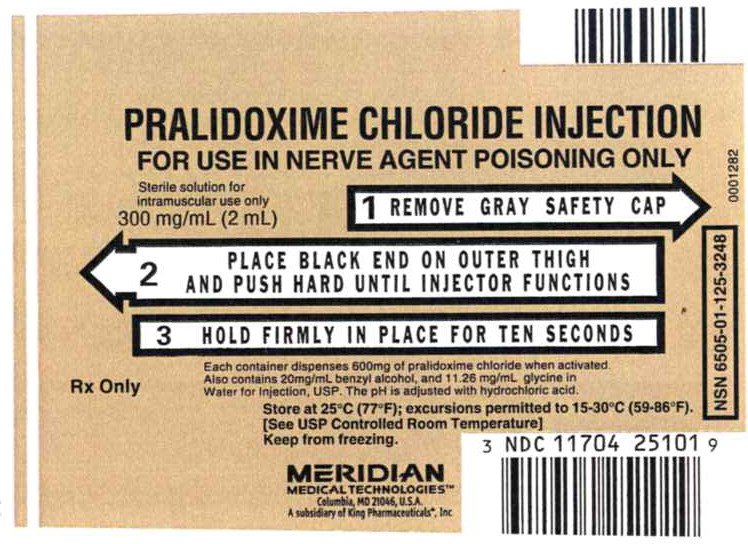
Panel de visualización Principal – Inyección de cloruro de Pralidoxima, Etiqueta de 300 mg
NDC 11704-107-01
Inyección DE cloruro de Pralidoxima
SOLO PARA USO EN INTOXICACIONES POR AGENTES NERVIOSOS
Solución estéril solo para uso intramuscular
300 mg/ml (2 ml)
1 RETIRE LA TAPA DE SEGURIDAD GRIS
2 COLOQUE EL EXTREMO NEGRO EN LA PARTE EXTERIOR DEL MUSLO Y EMPUJE CON FUERZA HASTA QUE FUNCIONE EL INYECTOR
3 SUJÉTELO FIRMEMENTE EN SU LUGAR DURANTE DIEZ SEGUNDOS
Cada envase dispensa 600 mg de cloruro de Pralidoxima cuando se activa.
También contiene 20 mg/ml de alcohol bencílico, y 11.26 mg/ml de glicina en
Agua para inyección, USP. El pH se ajusta con ácido clorhídrico.
Solo Rx
Almacenar a 25°C (77 ° F); se permiten excursiones a 15-30°C (59-86°F).
Evitar la congelación.
MERIDIAN MEDICAL TECHNOLIGIESTM
Columbia, MD 21046, USA
A subsidiary of King Pharmaceuticals®, Inc
NDC 11704-251-01
NSN 6505-01-125-3248
| Pralidoxime Chloride Pralidoxime Chloride injection |
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
Labeler – Meridian Medical Technologies, Inc. (167671341)
| Establishment | |||
| Name | Address | ID/FEI | Operations |
| Meridian Medical Technologies, Inc. | 038889234 | MANUFACTURE(11704-251), ANALYSIS(11704-251) | |
| Establishment | |||
| Name | Address | ID/FEI | Operations |
| Meridian Medical Technologies, Inc. | 078808315 | MANUFACTURE(11704-251), LABEL(11704-251), PACK(11704-251) | |
| Establishment | |||
| Name | Address | ID/FEI | Operations |
| Meridian Medical Technologies, Inc. | 167671341 | MANUFACTURE(11704-251), LABEL(11704-251), PACK(11704-251), ANALYSIS(11704-251) | |
More about pralidoxime
- Side Effects
- During Pregnancy
- Dosage Information
- Drug Interactions
- En Español
- Drug class: antídotos
- Alertas de la FDA (1)
Recursos para el consumidor
- Información para el paciente
- Inyección de Pralidoxima (Lectura Avanzada)
Recursos profesionales
- Información de prescripción
- Pralidoxima (Consejo Profesional para el Paciente)
Otras marcas Cloruro de Protopam
Guías de tratamiento relacionadas
- Sobredosis de anticolinesterasa
- Intoxicación por Organofosforados
- Intoxicación por agentes nerviosos
Descargo de responsabilidad médico