Le premier médicament biologique, l’insuline humanisée (5,8 kDa), est devenu disponible en 1982 après l’avènement de la biotechnologie, et il a marqué une nouvelle ère dans l’industrie pharmaceutique. Les progrès modernes de la biotechnologie permettent des synthèses à grande échelle de produits biologiques d’une manière plus ou moins rentable. Après avoir commencé avec de grands peptides et des protéines recombinantes, les produits biologiques comprennent aujourd’hui un large éventail d’autres entités, telles que les anticorps, les anticorps monoclonaux et, plus récemment, les nanobodies et objets apparentés, les récepteurs solubles, l’ADN recombinant, les conjugués anticorps-médicaments (ADC), les protéines de fusion, les immunothérapies et les vaccins synthétiques.
L’étoile montante des médicaments biologiques attire de plus en plus l’attention des professionnels pharmaceutiques et des analystes de l’industrie, car ce paradigme de découverte de médicaments alternatifs représente un défi commercial important pour le paradigme de découverte de médicaments à petites molécules plus traditionnel définissant l’industrie pharmaceutique depuis plus d’un siècle.
La question se pose donc: les petites molécules perdent-elles leur « attractivité » en tant qu’objets de recherche pour la découverte de médicaments dans le monde moderne des progrès biologiques? Certains experts restent optimistes quant au potentiel des petites molécules pour mener la course dans les futurs pipelines pharmaceutiques, d’autres perçoivent que « l’argent change de poches » et que la recherche sur les petites molécules sera de plus en plus négligée par les actionnaires et les investisseurs en faveur des produits biologiques.
Pour savoir où se dirige l’industrie, commençons d’abord par un peu de statistiques. Sur une période de 7 ans (2010-2017) États-Unis La Food and Drug Administration (FDA) a approuvé un total de 262 nouvelles entités moléculaires (NME), à l’exclusion de plusieurs agents d’imagerie diagnostique et de 1 analogue d’insuline (ref). Il apparaît que 76 % d’entre elles sont de petites molécules (199) dont seulement un quart sont des produits biologiques. Il est intéressant de noter qu’il n’y a pas de croissance apparente des approbations de produits biologiques NMEs par rapport aux petites molécules, car les deux catégories de produits thérapeutiques ont une tendance assez similaire, comme le montre le diagramme ci-dessous. Cependant, étant donné que les prix des produits biologiques sont très différents de ceux des petites molécules (ils sont beaucoup plus chers), la situation est différente lorsqu’on regarde la croissance totale des ventes et des revenus: sur la période de 2011 à 2017, les revenus des ventes de produits biologiques ont augmenté de 70% après avoir atteint 232 milliards de dollars. La part du marché pharmaceutique total détenue par les produits biologiques est passée de 16 % en 2006 à 25 % en 2016, sans signe apparent de ralentissement (ref).
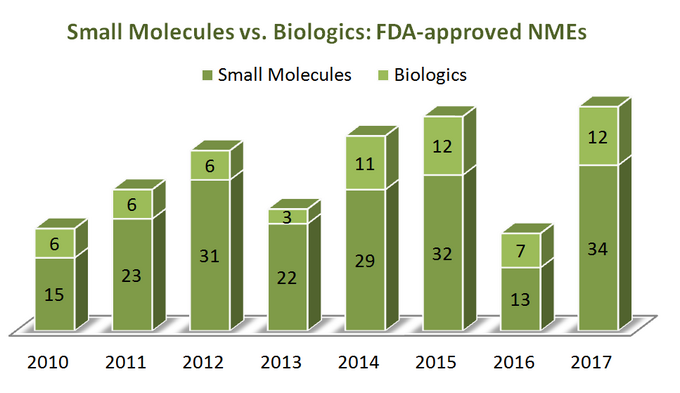
Bien qu’il existe des avantages distinctifs des produits biologiques par rapport aux petites molécules de plusieurs façons (par exemple, leur sélectivité profonde), les choses ne sont pas « en noir et blanc » lorsqu’on compare ces deux catégories de produits thérapeutiques par leurs attributs, car les deux ont des avantages et des inconvénients importants à prendre en compte lors de la prise de décision stratégique. Il semble donc un peu regrettable de voir à quel point de nombreux rapports ont écarté les SMS par rapport aux produits biologiques dans une quête de « fraîcheur » de leurs points de vue.
Un tableau ci-dessous résume certains aspects forts et faibles des deux catégories (ref, ref) illustrant les défis et les opportunités disponibles dans les deux « camps » (notez les couleurs: gris — aucun avantage apparent dans aucun des deux camps; vert situation situation avantageuse; jaune situation situation désavantageuse):
Petites molécules |
Produits biologiques |
|---|---|
|
Propriétés générales |
|
|
Poids moléculaires faibles (0,1-1 kDa); généralement stables chimiquement et thermiquement, large gamme de polarité. |
Poids moléculaires très importants> 1 kDa; généralement polaire, sensible à la chaleur, facilement dégradable (à l’exception de certains types à longue durée de vie tels que les anticorps monoclonaux) |
|
Sélectivité, sécurité |
|
|
Plutôt promiscuous, se lient généralement vers divers sites hors cible, produisant des effets secondaires ou une toxicité. Enfin, les développeurs de produits biologiques ont eu plus de facilité à obtenir des brevets car il y avait peu ou pas d’état de l’art dans le domaine, lorsque les blockbusters actuels ont été découverts. |
Hautement spécifique aux cibles, généralement de toxicité inférieure (à une exception majeure étant celle de l’immunogénicité, qui peut sérieusement influencer l’efficacité, l’innocuité et la disposition des produits biologiques). |
|
Perméabilité cellulaire |
|
|
Les SMS se lient à des cibles telles que les récepteurs couplés aux protéines G (RCPG), les canaux ioniques à chaîne ligand et les tyrosines kinases des récepteurs sur les récepteurs extracellulaires ou domaines intracellulaires. Ils peuvent accéder à des cibles dans les régions intracellulaires, les cytosols, les noyaux et même les cibles du SNC, séparées par la barrière hémato-encéphalique serrée (BBB). |
Une grande partie des cibles pharmacologiques sont intégrées et donc inaccessibles aux produits biologiques. En particulier, en ce qui concerne le système nerveux central (SNC), la présence de la barrière hémato-encéphalique est un obstacle majeur sur le chemin de toute molécule de plus de 600 Da limitant jusqu’à 98% des SMS et pratiquement tous les produits biologiques. |
|
Livraison |
|
|
Tombent en grande partie dans la « règle des cinq » pour l’absorption orale, ce qui le rend approprié pour l’administration orale. La perméabilité supplémentaire via l’épithélium intestinal est principalement médiée par une combinaison de diffusion passive et de transport paracellulaire. |
L’instabilité intrinsèque et les masses moléculaires élevées rendent presque tous les produits biologiques inactifs par voie orale. Principalement, la livraison invasive, ou des technologies alternatives non invasives en cours. |
|
Distribution |
|
|
Les SMS sont distribués via la circulation sanguine, ce qui permet d’atteindre rapidement les concentrations de prélèvement. |
Pour les molécules plus grosses (par exemple > 10 kDa), un système lymphatique plus lent (de 100 à 500 fois) devient dominant dans le processus de distribution. Les produits biologiques de plus grande taille se distribuent à la fois dans le sang et dans les systèmes lymphatiques en mouvement de transport convectif, d’endocytose médiée par les récepteurs, de phagocytose et de pinocytose. Le résultat de cette situation est que les produits biologiques de plus grande taille ont une demi-vie plus longue, des volumes de distribution limités et ont besoin de plus de temps pour atteindre les concentrations maximales, par rapport aux SGS. |
|
Disposition (métabolisme) |
|
|
La plupart des SMS sont éliminés par des organes non ciblés via via des métabolismes cytochromes ou non cytochromes, une filtration rénale ou une excrétion fécale. |
Les produits biologiques ont des interactions plus étroites avec les cibles, de sorte que leurs dispositions sont directement affectées par leur liaison (disposition du médicament médiée par les récepteurs), y compris les dégagements des produits biologiques par les protéases et les peptidases. |
|
Interactions médicament-médicament |
|
|
Les SMS sont sujets à des interactions médicament–médicament pouvant survenir en raison de la présence de médicaments concomitants qui affectent leurs voies de transport, de métabolisme, de transport ou d’élimination. |
Les produits biologiques sont moins sujets aux interactions médicamenteuses traditionnelles puisqu’ils subissent un métabolisme et une élimination en tant que substrats endogènes. Cependant, il existe des changements documentés médiés par les cytokines dans les enzymes métabolisant les médicaments, par conséquent, les interactions médicament-biologique doivent être évaluées dans le cas où le médicament pourrait influencer l’expression des enzymes métaboliques. |
|
Aspects commerciaux |
|
|
Prix bas pour les médicaments SM. |
En règle générale, les prix des traitements biologiques sont très élevés. Cela est considéré comme l’une des raisons pour lesquelles les produits biologiques semblent offrir de meilleurs rendements économiques globaux, comparativement aux SGS. |
|
Taux d’attrition élevé (une étude réalisée en 2009 par le groupe KMR a montré que seulement 7,1% des SMS entrant dans les tests précliniques ont finalement atteint le marché). |
Taux d’attrition relativement faible (la même étude du groupe KMR a révélé que 24,4 % des produits biologiques au stade préclinique ont survécu jusqu’au stade de commercialisation). |
|
Severe competition from chemical generics after patents expiration. |
Biologics developers face less severe competition from biosimilars, after patents expiration. |
|
Simpler drug discovery/development process. |
More expensive and complex drug discovery and development process, compared to biologics. |
Compte tenu de la comparaison ci-dessus, il devient évident que les produits biologiques ne sont pas une « solution miracle » et que l’industrie ne sera pas dominée par les produits biologiques dans un avenir prévisible, un équilibre concurrentiel sera plutôt maintenu entre les petites molécules, les produits biologiques et les formes hybrides de thérapeutiques, telles que les ADC with avec des domination de chaque forme dans des domaines thérapeutiques plus appropriés, des cas d’utilisation, etc.
En outre, voici une liste de plusieurs moteurs industriels qui jouent du côté des petites molécules et pourraient influencer l’équilibre des pouvoirs sur l’ensemble du marché pharmaceutique en faveur des points de départ chimiques :
L’essor de l’intelligence artificielle (IA) dans la découverte de médicaments
Suite aux percées des algorithmes d’apprentissage profond (2012) et plus récemment, la création de réseaux antagonistes génératifs (GAN), capables d’exceller dans un certain nombre de tâches de recherche, l’intérêt pour diverses technologies d’IA a explosé en à peu près toutes les industries. De nombreux outils alimentés par l’IA sont rapidement devenus courants commerciaux, tels que les chatbots, les assistants personnels, les pilotes automatiques, etc.– ce qui est une preuve de concept réelle de faisabilité de l’IA.
La découverte de médicaments ne fait pas exception à cette « tendance axée sur l’IA », et le nombre de startups qui tentent d’appliquer l’IA pour stimuler la découverte de médicaments de différentes manières a considérablement augmenté en quelques années, atteignant plus d’une centaine d’entreprises actives à ce jour (voici une liste de certaines d’entre elles).
Il est intéressant de noter que la majorité des startups axées sur l’IA se concentrent sur la découverte de médicaments de petites molécules, plutôt que sur les produits biologiques, ce qui n’est probablement pas surprenant. Historiquement, même les méthodes de calcul non basées sur l’IA (chemininformatique) étaient principalement utilisées pour les thérapies à petites molécules en raison de leurs structures moléculaires et de leurs schémas d’interaction considérablement plus simples.
Le diagramme ci-dessous montre une estimation des statistiques de 61 start-up de découverte de médicaments activement commercialisés développant ou appliquant des outils d’IA spécialisés dans leur flux de travail de recherche. Comme vous pouvez le constater, la moitié des entreprises (51%, 31 startups) se concentre sur les petites molécules, alors que seulement 23% (14 startups) sont impliquées dans la découverte / le développement de médicaments biologiques (anticorps, vaccins, etc.). La disproportion vis-à-vis des petites molécules est également bien illustrée par le montant des fonds de capital-risque collectés collectivement par 61 startups examinées axées sur l’IA (tournées divulguées publiquement uniquement) – où 770 millions ont été investis dans les entreprises impliquées dans les petites molécules et seulement un peu plus de 200 millions ont été alloués aux startups axées sur les produits biologiques – comme indiqué ci-dessous.
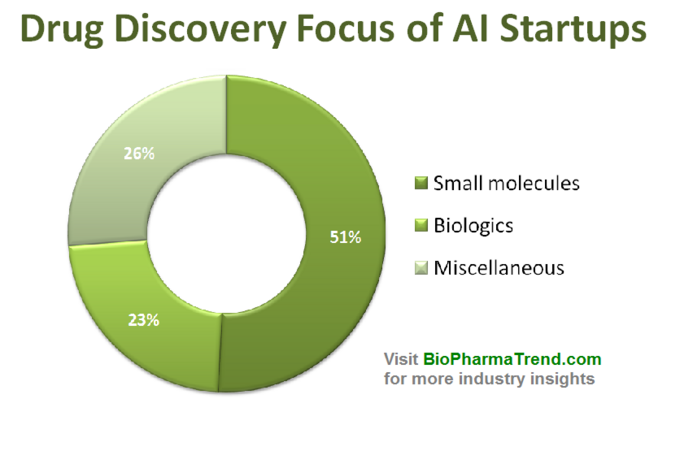
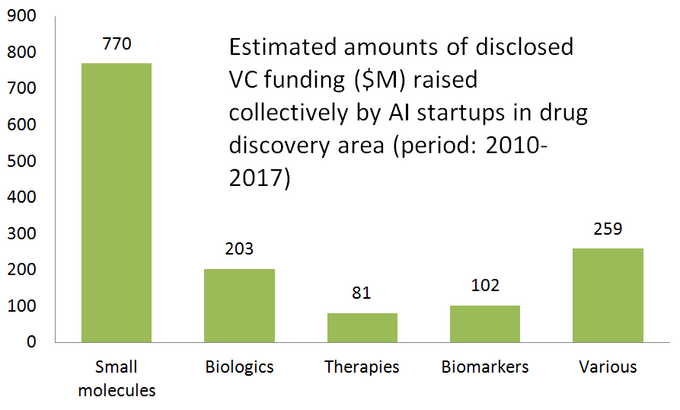
Cette situation suggère que les progrès récents des algorithmes d’IA et la tendance à appliquer l’apprentissage automatique à la recherche pharmaceutique à un stade précoce ont tendance à entraîner une plus grande croissance de la découverte de médicaments à petites molécules, par rapport à la découverte de produits biologiques — du moins pour l’instant. Cela pourrait conduire à davantage d’investissements futurs dans de petits projets axés sur les molécules soutenus par des technologies axées sur l’IA.
Atteindre des cibles « non contrôlables »
Des cibles aussi importantes que, par exemple, les interactions protéine-protéine (IPP), sont traditionnellement dominées par les produits biologiques (MAB) en tant qu’acteurs potentiels, alors que les petites molécules ont longtemps été considérées comme inadaptées dans ce cas en raison de leur petite taille.
Avec les progrès de la pharmacogénomique, cette situation peut évoluer assez rapidement suite aux homologations maraviroc (514 Da) et tirofiban (441 Da). Il a été révélé par calcul que les SMS peuvent en fait avoir des affinités relativement élevées avec des interfaces spécifiques de protéines et, surtout, qu’ils peuvent moduler les « régions protéiques intrinsèquement désordonnées » liées à un ensemble de maladies de systèmes complexes. Voici une couverture intéressante de ce sujet résumant certaines des informations importantes sur les machines PPI obtenues au cours des dernières décennies.
Un autre domaine en croissance rapide pour la découverte de médicaments à petites molécules est le ciblage de l’acide ribonucléique (ARN). Ce sujet a été répertorié dans « Top 7 Tendances de la recherche pharmaceutique en 2018″ » et il y avait également un examen détaillé du sujet en Biologie chimique cellulaire et une belle couverture de l’industrie dans C&EN.
Une autre idée nouvelle de libérer le pouvoir des petites molécules a été discutée dans un article récent « Les dégradants de protéines ciblées redéfinissent l’apparence et l’action des petites molécules » publié dans C&EN 2018. La stratégie ici est de développer de petites molécules bifonctionnelles capables d’acheminer une protéine ciblée vers le protéasome, la machine d’élimination des déchets de la cellule, au lieu d’inhiber simplement l’action de la protéine comme dans une approche « traditionnelle ».
Surmonter les limites des technologies de criblage
Beaucoup de potentiel de recherche sur les petites molécules n’a pas encore été réalisé en raison des diverses limites technologiques des approches de criblage utilisées pour identifier les points de départ des programmes de découverte de médicaments.
Un tel exemple est l’approche de dépistage phénotypique, qui connaît une renaissance de nos jours en raison de plusieurs avancées technologiques, y compris la capacité croissante de développer des modèles cellulaires physiologiquement pertinents, des lectures et des technologies de détection sophistiquées aidant à révéler les mécanismes d’action (MoA) plus efficacement, minimisant l’incertitude. D’autre part, la mise en œuvre de techniques de profilage et de méthodes de calcul à grande échelle offre un nouveau niveau d’analyse des systèmes et de compréhension des phénotypes de petites molécules.
Un autre paradigme de dépistage prometteur consiste à utiliser des bibliothèques codées par ADN (DELs). Grâce à son agencement unique, la technologie DEL offre un moyen approprié de tester des centaines de millions, voire des milliards de nouvelles molécules, dans le cadre de programmes de découverte de médicaments ciblés. Bien que cette technologie ne soit pas sans défis (par exemple, limites de la chimie compatible avec l’ADN, incertitude avec les résultats du dépistage, etc.), la zone se développe rapidement et est même considérée comme « révolutionnaire » pour la découverte de médicaments à petites molécules.
Surmonter la barrière de la synthétisabilité
L’une des pierres d’achoppement de la découverte précoce de médicaments à petites molécules est une limitation de l’espace chimique synthétiquement accessible while alors que de nombreuses idées chimiques prometteuses peuvent être générées par calcul, ou autrement, il y a toujours un risque que la synthèse de l’ensemble des composés pour valider de telles idées soit coûteuse, voire irréalisable.
Des progrès récents dans ce domaine ont été réalisés, encore une fois, en utilisant un logiciel basé sur l’IA offrant des performances de planification de synthèse au niveau humain. Par exemple, BenevolentAI a récemment publié un article dans Nature, décrivant comment ils utilisaient des réseaux de neurones profonds en combinaison avec des algorithmes de recherche d’arbres modernes pour planifier la synthèse de nouvelles molécules avec un taux de réussite et une vitesse remarquables.
Plusieurs couvertures intéressantes avec de riches commentaires ont été publiées ici et ici par Derek Lowe, fournissant un peu plus d’informations sur ce domaine fascinant de la chimie organique et médicinale.
Une stratégie plus empirique a été développée par un producteur chimique Enamine, connu sous le nom d’Espace chimique RÉEL, et comprend actuellement plus de 3.8 milliards de molécules synthétiquement accessibles et consultables pour l’exploration hit et d’autres tâches de chimie médicinale. Le concept se résume à appliquer un ensemble de voies chimiques validées en interne (plus de 100 réactions) à un grand nombre de blocs de construction chimiques disponibles en stock (plus de 100 000 composés) — dans le but de les combiner de manière combinatoire pour produire une cascade de molécules plus grandes « ressemblant à du plomb » ou « ressemblant à des médicaments ». Une fois qu’un certain degré de reproductibilité et de rendement est atteint dans un ensemble d’expériences suffisamment important (au moins 80%), une nouvelle énumération informatique a lieu pour constituer un espace chimique plus large basé sur les cas validés expérimentalement.
New R&D marchés et rôles des petites molécules
Dans l’ensemble, on peut ignorer ou mal comprendre la taille et le potentiel de croissance des pipelines de petites molécules, comme cela a été mentionné lors d’une table ronde à Interphex. Actuellement, environ 8000 petites molécules sont actives dans R&D, soit une croissance de 25% au cours des deux dernières années. Les facteurs de croissance énumérés ci-dessus pourraient conduire à une nouvelle accélération de la croissance dans ce secteur.
Il est également important de noter que les médicaments à petites molécules pourraient jouer un rôle important dans certains médicaments de nouvelle génération, les rendant dépendants de petits pipelines de molécules. Par exemple, dans le cas de la thérapie par cellules souches, de petites molécules peuvent déclencher des réactions thérapeutiques.
Comme l’a souligné Jeffrey Shumway de MilliporeSigma lors de l’ICsP Amérique du Nord, les produits à petites molécules tendent à devenir plus complexes, modifiant leur rôle dans l’industrie (bio)pharmaceutique.
Enfin, le domaine futur des petites molécules est celui des conjugués anticorps-médicament et des objets apparentés, qui sont apparus comme une classe de thérapeutiques prometteuses en raison de la convergence naturelle de deux paradigmes de découverte de médicaments et de multiples tendances technologiques.
Avertissement: L’information est uniquement destinée à la sensibilisation générale et n’est pas un conseil juridique / financier / boursier / médical de quelque nature que ce soit. Vous le lisez à votre guise et toute utilisation de ces informations est à vos risques et périls. Il est de votre responsabilité d’évaluer l’utilité et la sécurité des informations contenues dans ce post, et Internet en général, et comment elles s’appliquent à votre propre situation, puis de consulter les experts compétents pour obtenir des conseils professionnels si nécessaire.
Sujets : Tendances de l’industrie