forma de dozare: injecție
Medical revizuite de Drugs.com. Ultima actualizare pe 22 mai 2020.
- Overview
- Side Effects
- Dosage
- Professional
- Interactions
- More
FOR USE IN NERVE AGENT POISONING ONLY
A Sterile Solution For Intramuscular Use Only
Rx Only
- Pralidoxime Chloride Description
- clorură de Pralidoximă – Farmacologie Clinică
- indicații și utilizare pentru clorura de Pralidoximă
- contraindicații
- avertismente
- Precauții
- General:
- informații pentru pacienți:
- teste de laborator:
- interacțiuni medicamentoase:
- carcinogeneză, Mutagensis, afectarea fertilității:
- sarcina
- mamă care alăptează:
- utilizare pediatrică:
- reacții Adverse
- abuzul de droguri și dependența
- supradozaj
- manifestări de supradozaj:
- tratamentul supradozajului:
- Acute Toxicity:
- dozare și administrare de clorură de Pralidoximă
- instrucțiuni de Utilizare:
- cum este furnizată clorura de Pralidoximă
- Panou principal de afișare – injecție de clorură de Pralidoximă, etichetă de 300 mg
- mai multe despre pralidoximă
- resurse pentru consumatori
- resurse profesionale
- ghiduri de tratament conexe
Pralidoxime Chloride Description
Pralidoxime Chloride Injection (auto-injector) provides Pralidoxime Chloride in a sterile solution for intramuscular injection.
fiecare autoinjector preumplut furnizează o doză de antidot, clorură de Pralidoximă într-o unitate autonomă, special concepută pentru autoadministrarea automată sau amică de către personalul militar. Pralidoxima în autoinjector poate fi, de asemenea, administrată de către personalul de intervenție civilă calificat, care a avut o pregătire adecvată în recunoașterea la fața locului și în tratamentul intoxicației cu neurotoxină în cazul unei eliberări accidentale de neurotoxină. Procedura recomandată (vezi dozare și administrare) este de a injecta conținutul autoinjectorului în mușchii coapsei exterioare.
după ce un autoinjector a fost activat, recipientul gol trebuie aruncat în mod corespunzător (vezi dozare și administrare), nu poate fi reumplut și nici acul proeminent nu poate fi retras.
când este activat, fiecare autoinjector eliberează 600 mg clorură de Pralidoximă în 2 mL soluție sterilă conținând 20 mg/mL alcool benzilic, 11,26 mg/mL glicină în apă pentru preparate injectabile, USP. PH-ul este ajustat cu acid clorhidric. Intervalul de pH este de 2,0-3,0. Produsul nu conține pirogeni.
clorura de Pralidoximă este un reactivator al colinesterazei.
denumirea chimică: Clorură de 2-formil-1 metilpiridiniu oximă (metoclorură de piridină-2-aldoximă). Denumită și clorură de 2-PAM.
Formula structurală:
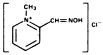
clorura de Pralidoximă apare ca o pulbere cristalină inodoră, albă, nehigroscopică, care este solubilă în apă până la 1 g în mai puțin de 1 mL. Stabil in aer, se topeste intre 215 si 225, cu descompunere.
activitatea specifică a medicamentului constă în ionul 2-formil-1 metilpiridiniu și este independentă de sarea particulară utilizată. Clorura este preferată datorită compatibilității fiziologice, solubilității excelente în apă la toate temperaturile și potenței ridicate pe gram, datorită greutății sale moleculare scăzute (173).
clorură de Pralidoximă – Farmacologie Clinică
clorura de Pralidoximă este un reactivator al colinesterazei.acțiunea principală a pralidoximei este reactivarea colinesterazei (în principal în afara sistemului nervos central) care a fost inactivată prin fosforilare datorită unui pesticid organofosfat sau a unui compus înrudit. Distrugerea acetilcolinei acumulate poate continua și joncțiunile neuromusculare vor funcționa din nou în mod normal. Pralidoxima încetinește, de asemenea, procesul de „îmbătrânire” a colinesterazei fosforilate într-o formă care nu poate fi reactivată și detoxifică anumiți organofosfați prin reacție chimică directă. Medicamentul are efectul său cel mai critic în ameliorarea paraliziei mușchilor respirației. Deoarece pralidoxima este mai puțin eficientă în ameliorarea depresiei centrului respirator, atropina este întotdeauna necesară concomitent pentru a bloca efectul acetilcolinei acumulate la acest loc. Pralidoxima ameliorează semnele și simptomele muscarinice, salivația, bronhospasmul etc., dar această acțiune este relativ neimportantă, deoarece atropina este adecvată în acest scop.
Pralidoxima este distribuită în toată apa extracelulară, nu se leagă de proteinele plasmatice. Medicamentul este excretat rapid în urină parțial neschimbat și parțial ca metabolit produs de ficat. În consecință, pralidoxima are o acțiune relativ scurtă și pot fi necesare doze repetate, în special acolo unde există dovezi ale absorbției continue a otrăvii.
concentrația terapeutică minimă de pralidoximă în plasmă este de 4 hectolitri / mL, acest nivel fiind atins în aproximativ 16 minute după o singură injecție de clorură de Pralidoximă 600 mg. Timpul de înjumătățire aparent al clorurii de Pralidoximă este de 74-77 minute.
s-a raportat că utilizarea suplimentară a reactivatorilor de colinesterază oximă (cum ar fi pralidoxima) reduce incidența și severitatea defectelor de dezvoltare la embrionii de pui expuși la teratogeni cunoscuți precum paration, bidrin, carbachol și neostigmină. Acest efect protector al oximelor s-a dovedit a fi dependent de doză.
indicații și utilizare pentru clorura de Pralidoximă
acest autoinjector pentru clorura de Pralidoximă este indicat în mod specific pentru utilizare intramusculară ca adjuvant la atropină în tratamentul otrăvirii cu agenți nervoși cu activitate anticolinesterazică.
contraindicații
autoinjectorul de clorură de Pralidoximă este contraindicat la pacienții hipersensibili la orice componentă a produsului.
avertismente
Pralidoxima nu este eficientă în tratamentul otrăvirii datorită fosforului, fosfaților anorganici sau organofosfaților care nu au activitate anticolinesterazică.
Precauții
General:
Pralidoxima a fost foarte bine tolerată în majoritatea cazurilor, dar trebuie amintit că starea disperată a pacientului otrăvit cu organofosfat va masca, în general, semnele și simptomele minore observate la subiecții normali.
deoarece pralidoxima este excretată în urină, o scădere a funcției renale va duce la creșterea nivelului sanguin al medicamentului. Astfel, doza de pralidoximă trebuie redusă în prezența insuficienței renale.
informații pentru pacienți:
autoinjectorul de clorură de Pralidoximă trebuie să fie administrat de personal militar sau de personal civil calificat pentru intervenții de urgență numai după ce au avut loc următoarele evenimente:
– individul și – a îmbrăcat masca după recunoașterea existenței unui pericol de agent chimic în zona sa- unele sau toate simptomele otrăvirii cu agenți nervoși citate mai jos sunt prezente: secreții nazale inexplicabile senzație de constricție toracică cu dificultate în respirație pupilele oculare identificate, care duc la vedere încețoșată Salivare, transpirație excesivă greață, vărsături și crampe abdominale urinare involuntară și defecare Convulsie, spasme și dureri de cap uluitoare, somnolență, comă, convulsii oprirea respirației
trebuie luate măsuri adecvate pentru a se asigura că personalul echipat cu autoinjectoare înțelege indicațiile și utilizarea acestora, inclusiv revizuirea simptomelor de otrăvire și funcționarea autoinjectorului.
teste de laborator:
tratamentul otrăvirii cu organofosfat trebuie instituit fără a aștepta rezultatele testelor de laborator. Măsurătorile de celule roșii din sânge, colinesterază plasmatică și paranitrofenol urinar (în cazul expunerii la paration) pot fi utile în confirmarea diagnosticului și urmărirea evoluției bolii. O reducere a concentrației de colinesterază a globulelor roșii la Sub 50% din normal a fost observată numai în cazul otrăvirii cu ester organofosfat.
interacțiuni medicamentoase:
când atropina și pralidoxima sunt utilizate împreună, semnele de atropinizare (înroșirea feței, midriază, tahicardie, uscăciunea gurii și nasului) pot apărea mai devreme decât s-ar putea aștepta atunci când atropina este utilizată singură. Acest lucru este valabil mai ales dacă doza totală de atropină a fost mare și administrarea de pralidoximă a fost întârziată.2, 3, 4
următoarele precauții trebuie luate în considerare în tratamentul otrăvirii cu anticholesterinază, deși nu suportă direct utilizarea pralidoximei; deoarece barbituricele sunt potențate de anticholinesteraze, acestea trebuie utilizate cu precauție în tratamentul convulsiilor; morfina, teofilina, aminofilina, succinilcolina, reser-pinul și tranchilizantele de tip fenotiazină trebuie evitate la pacienții cu otrăvire cu organofosfat.
carcinogeneză, Mutagensis, afectarea fertilității:
deoarece autoinjectorul cu clorură de Pralidoximă este indicat numai pentru utilizare de urgență pe termen scurt, producătorul nu a efectuat investigații privind potențialul său de carcinogeneză, mutageneză sau afectare a fertilității sau nu a fost raportat în literatura de specialitate.
sarcina
nu s-au efectuat studii privind reproducerea la animale cu pralidoximă. De asemenea, nu se știe dacă pralidoxima poate provoca leziuni fetale atunci când este administrată unei femei însărcinate sau poate afecta capacitatea de reproducere. Pralidoxima trebuie administrată unei femei gravide numai dacă este absolut necesar.
mamă care alăptează:
nu se știe dacă acest medicament este excretat în laptele uman. Deoarece multe medicamente sunt excretate în laptele uman, trebuie să aveți precauție atunci când pralidoxima este administrată unei femei care alăptează.
utilizare pediatrică:
siguranța și eficacitatea la copii nu au fost stabilite.
reacții Adverse
la patruzeci până la 60 de minute după injectarea intramusculară, la locul injectării pot apărea dureri ușoare până la moderate.
Pralidoxima poate provoca vedere încețoșată, diplopie și tulburări de acomodare, amețeli, dureri de cap, somnolență, greață, tahicardie, creșterea tensiunii arteriale sistolice și diastolice, hiperventilație și slăbiciune musculară atunci când este administrată parenteral voluntarilor normali care nu au fost expuși la otrăvuri anticolinesterazice. La pacienți este foarte dificil să se diferențieze efectele toxice produse de atropină sau compușii organofosfați de cele ale medicamentului.
au fost observate creșteri ale concentrațiilor enzimelor SGOT și / sau SGPT la 1 din 6 voluntari normali cărora li s-a administrat 1200 mg clorură de Pralidoximă intramuscular și la 4 din 6 voluntari cărora li s-a administrat 1800 mg intramuscular. Nivelurile au revenit la normal în aproximativ 2 săptămâni. Creșteri tranzitorii ale creatinfosfokinazei au fost observate la toți voluntarii normali cărora li s-a administrat medicamentul. O singură injecție intramusculară de 330 mg în 1 mL la iepuri a provocat mionecroză, inflamație și hemoragie.
când atropina și pralidoxima sunt utilizate împreună, semnele de atropinizare pot apărea mai devreme decât s-ar putea aștepta atunci când atropina este utilizată singură. Acest lucru este valabil mai ales dacă doza totală de atropină a fost mare și administrarea de pralidoximă a fost întârziată.2, 3, 4 excitare și comportament maniacal imediat după recuperarea conștienței au fost raportate în mai multe cazuri. Cu toate acestea, un comportament similar a apărut în cazurile de otrăvire cu organofosfat care nu au fost tratate cu pralidoximă.3, 5, 6
abuzul de droguri și dependența
clorura de Pralidoximă nu este supusă abuzului și nu are potențial cunoscut de dependență.
supradozaj
manifestări de supradozaj:
observate numai la subiecții normali: amețeli, vedere încețoșată, diplopie, cefalee, tulburări de acomodare, greață, ușoară tahicardie. În terapie a fost dificil să se diferențieze efectele secundare datorate medicamentului de cele datorate efectelor otrăvii.
tratamentul supradozajului:
respirația artificială și alte terapii de susținere trebuie administrate după cum este necesar.
Acute Toxicity:
i.v.—man TDLo: 14 mg/kg (toxic effects: CNS) i.v.— rat LD50: 96 mg/kg i.m.—rat LD50: 150 mg/kg oral—mouse LD50: 4100 mg/kg i.p.—mouse LD50: 155 mg/kg i.v.—mouse LD50: 90 mg/kg i.m.—mouse LD50: 180 mg/kg i.v.—rabbit LD50: 95 mg/kg i.m.—guinea pig LD50: 168 mg/kg
dozare și administrare de clorură de Pralidoximă
expunerea la agenți nervoși cu activitate anticolinesterazică (tip organofosfat)
caz ușor—cefalee, vedere încețoșată, semne muscarinice ușoare
caz moderat sever—transpirație excesivă, lacrimare, Salivare, diaree, senzație de apăsare în piept
pentru reactivarea optimă a colinesterazei, atropinei și pralidoximei inhibate de organofosfat trebuie administrat cât mai curând posibil după expunere. În funcție de severitatea simptomelor, administrați imediat un autoinjector care conține atropină, urmat de un autoinjector care conține pralidoximă. Atropina trebuie administrată mai întâi până când efectele sale devin evidente și numai atunci trebuie administrată pralidoxima. Dacă simptomele agentului nervos sunt încă prezente după 15 minute, repetați injecțiile. Dacă simptomele există încă după încă 15 minute, repetați injecțiile pentru a treia oară. Dacă după al treilea set de injecții, simptomele rămân, nu mai dați antidoturi, ci solicitați ajutor medical.
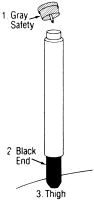
instrucțiuni de Utilizare:
când, așa cum este descris mai sus, este indicată utilizarea autoinjectorului, procedați după cum urmează:
|
 |
caz foarte sever — cianoza, jena respiratorie, coma
măsurile inițiale ar trebui să includă îndepărtarea secrețiilor, menținerea unei căi respiratorii brevetate și, dacă este necesar, ventilația artificială. Atropina nu trebuie utilizată până când cianoza nu a fost depășită, deoarece atropina produce fibrilații ventriculare în prezența hipoxiei. Morfina, teofilina, aminofilina sau succincilcolina sunt contraindicate. Tranchilizante de tip rezerpină sau fenotiazină trebuie evitate.
„Pralidoxima este cea mai eficientă dacă este administrată imediat după otrăvire. În general, se realizează puțin dacă medicamentul este administrat la mai mult de 36 de ore de la încetarea expunerii. Cu toate acestea, atunci când otrava a fost ingerată, expunerea poate continua o perioadă de timp din cauza absorbției lente din intestinul inferior, iar recidivele fatale au fost raportate după îmbunătățirea inițială. Administrarea continuă timp de câteva zile poate fi utilă la acești pacienți. Supravegherea atentă a pacientului este indicată timp de cel puțin 48 până la 72 de ore. Dacă a apărut expunerea cutanată, îmbrăcămintea trebuie îndepărtată și părul și pielea spălate bine cu bicarbonat de sodiu sau alcool cât mai curând posibil. Diazepamul poate fi administrat cu precauție dacă convulsiile nu sunt controlate de atropină.”7
IMPORTANT: medicii și / sau alt personal MEDICAL care asistă victimele evacuate ale agenților nervoși ar trebui să evite expunerea la contaminarea cu îmbrăcămintea victimelor.
cum este furnizată clorura de Pralidoximă
clorura de Pralidoximă este furnizată în soluție apoasă preumplută în autoinjector (600 mg, 2 mL) pentru uz militar și pentru utilizare de către personalul de intervenție civilă calificat în situații de urgență. Auto-injectoarele sunt furnizate prin Direcția de materiale medicale, Centrul de aprovizionare pentru apărare Philadelphia sau altă agenție locală, de stat sau federală analogă.
când este activat, fiecare autoinjector eliberează 600 mg clorură de Pralidoximă în 2 mL soluție sterilă conținând 20 mg/mL alcool benzilic, 11,26 mg/mL glicină în apă pentru preparate injectabile, USP. PH-ul este ajustat cu acid clorhidric. PH-ul este de 2,0-3,0 produsul nu conține pirogeni.
A se depozita la 25 CTF (77 CTF F); excursii permise la 15-30 CTF (59-86 CTF).
păstrați de la congelare.
Meridian Medical Technologies, Inc.
Columbia, MD 21046
O companie Pfizer
00001976
08/16
tipărită în S. U. A.
- Landauer, W.: tetrogeni colinomimetici. V. efectul oximelor și reactivatorilor de colinesterază înrudiți, Teratologie 15: 33 (Feb.) 1977.
- Moller, K. O., Jenson-Holm, J. și Lausen, H. H.: Ugeskr. Laeg.123:501, 1961.
- Namba, T., Nolte, C. T., Jackrel, Jr.și Grob, D.: otrăvire datorată insecticidelor organofosfatice. Manifestări Acute și cronice, Amer. J. Med. 50: 475 (Apr.) 1971.
- Arena, J. M.: otrăvire. Toxicologie. Simptome. Tratamente, ed. 4, Springfield, Bolnav., Charles C. Thomas, 1979, p.133.
- Brachfeld, J., și Zavon, M. R.: fosfat Organic (Fosdrin inktiv) intoxicație. Raportul de caz și rezultatele tratamentului cu 2-PAM, arh. Environ. Sănătate 11: 859,1965.
- Hayes, W. J., Jr.: Toxicologia pesticidelor, Baltimore, Williams& compania Wilkins, 1975, p.416.
- Departamentul de droguri AMA: evaluări de droguri AMA, ed. 4, Chicago, Asociația Medicală Americană, 1980, p. 1455.
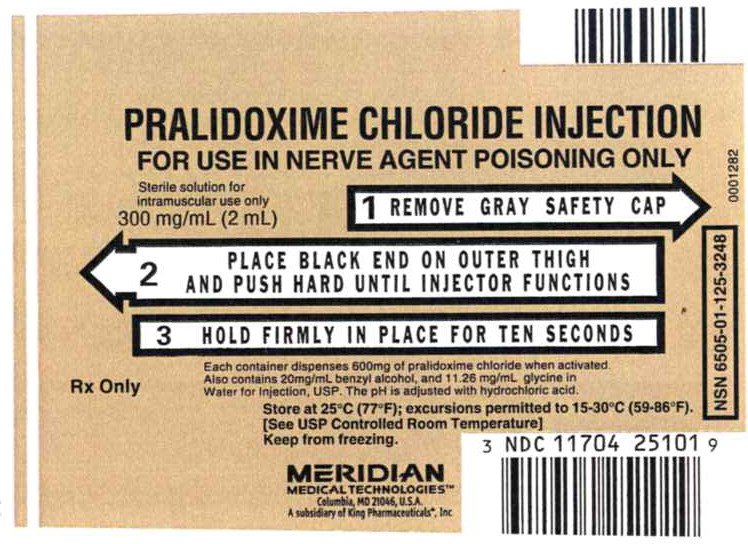
Panou principal de afișare – injecție de clorură de Pralidoximă, etichetă de 300 mg
NDC 11704-107-01
injecție de clorură de Pralidoximă
pentru utilizare numai în intoxicații cu agenți nervoși
soluție sterilă numai pentru utilizare intramusculară
300 mg/mL (2 mL)
1 Scoateți capacul gri de siguranță
2 Așezați capătul negru pe coapsa exterioară și împingeți puternic până când injectorul funcționează
3 țineți ferm în poziție timp de zece secunde
fiecare recipient eliberează 600 mg de clorură de pralidoximă atunci când este activat.
conține, de asemenea, 20 mg / ml alcool benzilic și 11.26 mg / mL glicină în
apă pentru preparate injectabile, USP. PH-ul este ajustat cu acid clorhidric.
numai Rx
A se depozita la 25 CTF (77 CTF); excursii permise la 15-30 CTF (59-86 CTF).
păstrați de la congelare.
MERIDIAN MEDICAL TECHNOLIGIESTM
Columbia, MD 21046, USA
A subsidiary of King Pharmaceuticals®, Inc
NDC 11704-251-01
NSN 6505-01-125-3248
| Pralidoxime Chloride Pralidoxime Chloride injection |
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
Labeler – Meridian Medical Technologies, Inc. (167671341)
| Establishment | |||
| Name | Address | ID/FEI | Operations |
| Meridian Medical Technologies, Inc. | 038889234 | MANUFACTURE(11704-251), ANALYSIS(11704-251) | |
| Establishment | |||
| Name | Address | ID/FEI | Operations |
| Meridian Medical Technologies, Inc. | 078808315 | MANUFACTURE(11704-251), LABEL(11704-251), PACK(11704-251) | |
| Establishment | |||
| Name | Address | ID/FEI | Operations |
| Meridian Medical Technologies, Inc. | 167671341 | MANUFACTURE(11704-251), LABEL(11704-251), PACK(11704-251), ANALYSIS(11704-251) | |
mai multe despre pralidoximă
- efecte secundare
- în timpul sarcinii
- informații privind dozajul
- interacțiuni medicamentoase
- En Espa Inktsol
- clasa de medicamente: antidoturi
- alerte FDA (1)
resurse pentru consumatori
- informații pentru pacienți
- injecție Pralidoximă (citire avansată)
resurse profesionale
- informații de prescriere
- Pralidoximă (sfaturi profesionale pentru pacienți)
Alte mărci clorură de Protopam
ghiduri de tratament conexe
- supradoză de anticolinesterază
- otrăvire cu organofosfat
- otrăvire cu agenți nervoși
Disclaimer Medical